Актуальность исследования
Иммуноцитохимическое исследование (ИЦХ) становится важным вспомогательным методом в цитологической диагностике онкологических заболеваний, поскольку традиционный цитоморфологический анализ далеко не всегда позволяет достоверно определить гистогенез опухолевых клеток и исключить диагностические ошибки при отсутствии характерных морфологических признаков. ИЦХ даёт возможность локализовать и выявить специфические антигены в цитологических препаратах с помощью меченых антител, что расширяет диагностические возможности классической цитологии и помогает уточнять происхождение, тип и потенциально злокачественный характер клеточных образцов.
Несмотря на то, что ИЦХ традиционно применяется шире в иммуногистохимии при исследовании тканей, его использование в цитологии приобретает всё большую значимость, особенно при диагностике опухолей с неопределёнными цитологическими заключениями и в ситуациях, когда морфологический анализ достигает своих пределов. Этот метод повышает точность диагностики, снижает долю неопределённых заключений и даёт дополнительные маркеры для дифференциальной диагностики сложных случаев.
Таким образом, интеграция иммуноцитохимии в рутинную цитологическую практику онкологических центров представляет собой актуальное направление современной патологической диагностики, направленное на повышение информативности, объективности и качества диагностики новообразований и оптимизацию клинического пути пациента.
Цель исследования
Целью данного исследования является анализ применения иммуноцитохимии в диагностике онкологических заболеваний, оценка её преимуществ и ограничений, а также исследование перспектив развития этого метода в клинической практике.
Материалы и методы исследования
Для исследования использованы данные литературы по применению иммуноцитохимических методов в клинической диагностике онкологических заболеваний, а также практические примеры использования маркеров в диагностике различных типов опухолей. Были проанализированы публикации по теме ИЦХ, включая работы по её использованию в рутинной клинической практике и перспективам её развития.
Результаты исследования
Иммуноцитохимическое исследование (ИЦХ) – это лабораторный метод, применяемый для выявления специфических антигенов в отдельных клетках с помощью меченых антител. Такой подход позволяет визуализировать белки, экспрессируемые в клеточных ядрах, цитоплазме или на мембране, и дает дополнительную информацию о биологическом статусе клеток, которую невозможно получить только на основе морфологии [3, с. 24].
Стандартный процесс ИЦХ включает фиксацию образца, последующее связывание с антителами, мечеными ферментами или флуорофорами, и визуализацию под микроскопом. Метод опирается на принцип антиген‑антитело и может выполняться с использованием прямого или непрямого способа окрашивания:
- прямой способ – меченое антитело связывается непосредственно с антигеном;
- непрямой способ – непрямое связывание первичного антитела с антигеном и последующая визуализация через вторичное меченое антитело, что обычно повышает чувствительность.
В качестве наглядного пособия для понимания процесса иммуноцитохимического исследования, на рисунке ниже представлена инфографика, иллюстрирующая этапы выполнения метода. На изображении чётко отображены ключевые стадии: от подготовки биологического материала до визуализации результатов под микроскопом.
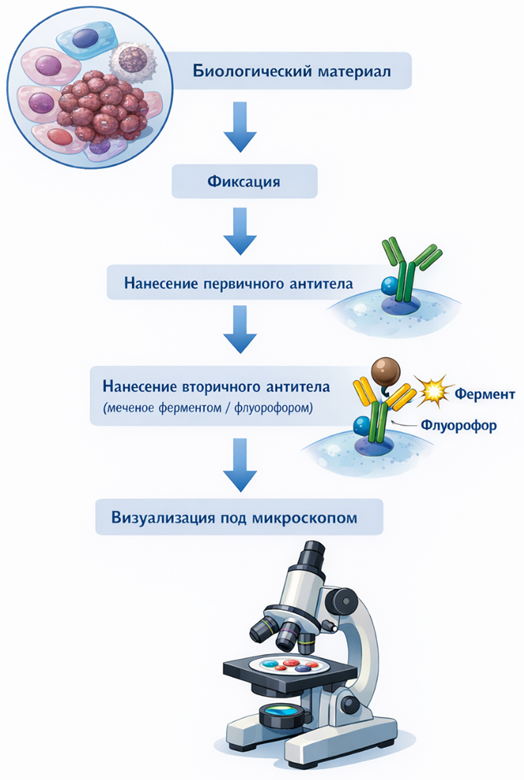
Рис. Схема принципа иммуноцитохимического окрашивания
Ниже приведена таблица 1 с часто используемыми иммуномаркерами, которые применяются в цитологических исследованиях онкологического материала. Эти маркеры помогают дифференцировать тип опухолевых клеток, оценивать их пролиферативную активность и связывать с клиническими характеристиками опухоли.
Таблица 1
Примеры иммуномаркеров, применяемых в цитологической диагностике онкологических заболеваний (данные таблицы основаны на примерах иммуномаркеров, описанных в источниках о методах иммуноцитохимии и онкологических маркерах)
Маркер | Клеточный/биологический признак | Клинико‑диагностическое значение |
p16^INK4a | Ингибитор циклин‑зависимой киназы (тормозит клеточный цикл) | Ассоциирован с высоко‑рисковыми HPV‑связанными поражениями, используется для диагностики высокостепеных дисплазий и карцином шейки матки |
Ki‑67 | Пролиферативный маркер | Отражает активность клеточного деления; помогает определить агрессивность опухоли |
CD20 | B‑лимфоцитарный антиген | Используется для идентификации В‑клеточных лимфом |
CD117 (c‑Kit) | Рецептор тирозинкиназы | Маркер желудочно‑кишечных стромальных опухолей (GIST) |
AFP (альфа‑фетопротеин) | Онкомаркер | Используется при диагостике гепатоцеллюлярной карциномы и опухолей желточного мешка |
Иммуноцитохимия широко используется в современной клинической диагностике онкологических заболеваний как вспомогательный инструмент, который помогает установить природу клеток, когда морфологические признаки не дают однозначного ответа. Этот метод особенно ценен в цитологической диагностике, поскольку позволяет определять клеточную линию происхождения опухоли и уточнять локализацию новообразования, а также оценивать прогностические и предиктивные маркеры опухолей [1].
ИЦХ стала распространённой практикой при диагностике опухолей лёгких, щитовидной железы, молочной железы, гинекологических опухолей, лимфом и метастатических поражений, когда в цитологическом материале отсутствует достаточная морфологическая информативность. В рутинной диагностике ИЦХ применяется в сочетании с цитоморфологией, что позволяет повысить точность диагностики и снизить количество неопределённых заключений.
В диагностической практике ИЦХ особенно ценится за способность подтверждать линейность опухолевых клеток – то есть определять, из какого типа ткани они происходят (эпителий, мезенхимальные элементы, лимфоидная ткань и др.). Это особенно важно в цитологии, где материал часто получен малоинвазивно (тонкоигольная пункция, соскобы, смывы), и стандартные морфологические признаки могут быть неоднозначны или неполными.
Кроме того, ИЦХ играет важную роль в оценке прогностических и предиктивных маркеров в онкологии. Например, оценка Ki‑67 позволяет судить о клеточной пролиферации и агрессивности опухоли, что важно для планирования лечения [5, с. 19].
Также стоит отметить, что в современных условиях клинические лаборатории всё чаще используют оптимизированные панели маркеров, адаптированные под конкретные диагностические ситуации, что делает ИЦХ неотъемлемой частью современного алгоритма диагностики злокачественных новообразований на основе цитологических образцов.
Иммуноцитохимическое исследование в клинической практике стало важным рутинным вспомогательным методом, позволяющим патологам повысить точность диагностики там, где морфологического анализа недостаточно. В современных цитологических лабораториях ИЦХ всё чаще применяется в сочетании с традиционными методами исследований, особенно когда требуется уточнить происхождение опухолевых клеток, определить тип опухоли или выявить специфические маркеры, значимые для выбора терапии.
Рутинное применение ИЦХ характерно для широкого круга онкологических патологий, включая опухоли лёгких, щитовидной железы, молочной железы, лимфоидные опухоли и неопределённые метастазы. Этот метод служит вспомогательным инструментом диагностического процесса и часто помогает подтвердить диагноз, особенно при тонкоигольной аспирационной биопсии (ТАБ) или других малоинвазивных цитологических пробах, когда материал ограничен и морфология клеток не даёт однозначного ответа [2, с. 6].
Важной частью рутинного применения ИЦХ является строгое соблюдение стандартов контроля качества и валидации методов, поскольку именно репродуцируемость и корректность выполнения обеспечивают достоверность результатов. Лаборатории обязаны иметь протоколы для контроля специфичности окраски и проверку качества на регулярной основе.
Ниже приведена таблица 2, отражающая примеры диагностических ситуаций, где ИЦХ используется как часть рутинной клинической практики, с указанием соответствующих маркеров и роли в диагностическом алгоритме.
Таблица 2
Примеры рутинного применения ИЦХ в клинической диагностике (анализ специализированной литературы по клиническому применению ICC/ИЦХ в цитологии)
Клиническая ситуация | Тип образца | Применяемые маркеры | Роль в рутинной диагностике |
Подтверждение неопределённого эпителиального происхождения опухоли | ТАБ лёгких, метастатический узел | CK7, CK20, TTF‑1 | Дифференциация аденокарциномы и неопределённых новообразований |
Подтипирование не‑мелкоклеточного рака лёгкого | Цитологические препараты | TTF‑1, Napsin A | Определение подтипа (аденокарцинома vs плоскоклеточный) |
Дифференциация фолликулярных образований щитовидной железы | ТАБ щитовидной железы | HBME‑1, Galectin‑3 | Повышение специфичности диагностики фолликулярной карциномы |
Диагностика лимфоидных новообразований | Лимфатические узлы | CD20, CD3, CD45 | Отличие лимфом от реактивных изменений |
Скрининг предраковых изменений шейки матки | Жидкостная цитология | p16 | Выявление высоко‑рисковых поражений, связанных с ВПЧ |
В рутинной практике ИЦХ также применяется для решения часто встречающихся диагностических дилемм, например:
- когда выявленные клетки имеют неоднозначные морфологические признаки и требуют уточнения их происхождения;
- при необходимости выделить прогностические маркеры (например, Ki‑67, p16, специфические рецепторы) для оценки прогноза заболевания или решения о лечении;
- при изоляции метастатических клеток в цитологических пробах, где первичный очаг неизвестен.
Для того чтобы ИЦХ действительно стала рутинным и эффективным методом, важно также обеспечить соответствующую подготовку персонала, регулярный контроль качества и установленные требования к интерпретации результатов, так как интерпретация окрашивания требует клинической квалификации и сопоставления с морфологическими признаками.
Иммуноцитохимическое исследование, несмотря на свою широкую интеграцию в рутинную диагностику, продолжает активно развиваться под влиянием прогресса в научных и технологических областях. Одним из ключевых направлений дальнейшего совершенствования ИЦХ является использование новых маркеров и методов, которые способны повысить чувствительность и специфичность диагностики, а также расширить функциональные возможности применяемых панелей антител. В частности, исследования в области оценки двойной экспрессии маркеров, таких как p16/Ki‑67, демонстрируют перспективу создания более объективных критериев верификации предраковых изменений, что особенно актуально для диагностики интраэпителиальных поражений шейки матки и других эпителиальных новообразований [4, с. 1589].
Важное направление развития связано с усовершенствованием технологий для работы с цитологическими образцами, таких как «клеточный блок» и современные подходы к жидкостной цитологии. Эти методы позволяют получать более качественные препараты для ИЦХ, включая возможность анализа серийных срезов с сопоставлением морфологических данных и результатов иммунной окраски на одном материале. Такое сочетание морфологии и ИЦХ повышает достоверность диагностики и способствует стандартизации интерпретации результатов в клинической практике.
Технологические инновации, разработка автоматизированных платформ и цифровизация диагностических процессов также играют существенную роль в будущем развития ИЦХ. Автоматизированные системы окрашивания уменьшают влияние человеческого фактора, повышают воспроизводимость и стандартизацию, что особенно важно при большом объёме анализов в современных лабораториях. Кроме того, технологии цифровой патологии и искусственного интеллекта открывают новые перспективы – интеграция ИИ‑алгоритмов в анализ изображений может облегчить интерпретацию окрашивания, повысить точность диагностики и ускорить процесс принятия клинических решений.
Одним из перспективных направлений является переход к мультиплексным ИЦХ, которые позволяют одновременно визуализировать несколько маркеров в одном образце. Это дает возможность получать более комплексную молекулярную информацию о биологии опухоли без увеличения объёма материала и сокращает количество необходимых реакций. Аналогичные подходы увеличивают диагностическую и прогностическую ценность ИЦХ при оценке сложных смешанных опухолей и при необходимости уточнения подтипов злокачественных процессов.
Перспективы также связаны с улучшением аналитических методов, включая усиление сигналов и новые способы мечения антител (например, с использованием наночастиц, квантовых точек и других инновационных меток), что позволяет обнаруживать белки с очень низкой экспрессией, ранее недоступные для стандартных методов. Это открывает новые возможности в ранней диагностике, когда опухолевая нагрузка минимальна и традиционные методы могут быть недостаточно чувствительными.
Наконец, будущее развития ИЦХ тесно связано с мультидисциплинарными подходами к диагностике онкологических заболеваний, где ИЦХ может сочетаться с молекулярными методами, такими как секвенирование и иммуно‑ПЦР, для более глубокого анализа опухолевых биомаркеров и предоставления мультиуровневых данных, необходимых для персонализированной медицины.
Выводы
Иммуноцитохимия является ключевым методом в диагностике онкологических заболеваний, который значительно повышает точность диагностики и даёт возможность точной дифференциации различных типов опухолей. Этот метод позволяет выявлять специфические антигены, которые служат индикаторами происхождения опухолевых клеток, а также помогает в оценке прогноза заболевания и выборе наиболее подходящей терапии. ИЦХ особенно полезна в случаях, когда традиционные методы цитологии не дают чёткого ответа или когда требуется подтверждение диагноза для более сложных и редких типов рака.
Несмотря на свои очевидные преимущества, ИЦХ имеет ряд ограничений, таких как зависимость от качества образцов, высокая стоимость и необходимость квалифицированной интерпретации результатов, что требует значительных ресурсов. Однако, с учётом новых технологий и улучшения методов окрашивания, а также интеграции с молекулярной диагностикой и цифровой патологией, этот метод продолжает развиваться, открывая новые перспективы для персонализированной медицины. В будущем, автоматизация и использование искусственного интеллекта в анализе ИЦХ-данных может значительно повысить точность диагностики и ускорить процесс принятия клинических решений, что сделает метод ещё более доступным и эффективным в повседневной клинической практике.
.png&w=384&q=75)
.png&w=640&q=75)