1. Введение
В начале – середине ⅩⅨ века эпидемиология сделала шаг в развитии на качественном уровне. Обобщив и применив накопившиеся со времён античности наблюдения, знания, технологии целеустремлённостью и талантом исследователей был создан и введён в практику метод вакцинации, ставший базовым, высокоэффективным по отношению к некоторым патогенным микроорганизмам обладающим собственным метаболизмом, методом эпидемиологии. Направление продолжает активно развиваться. Однако, возникновение, ход и итоги пандемии COVID-19 (2019–2023 г.) выявили недостаточность уровней эффективности и модернизационного потенциала известных методов и средств противодействия по отношению к вирусным воздушно-капельным инфекциям с повышенными значениями базового коэффициента репродукции (R₀ ≥ 2,5). Необходимы новации на качественном уровне. В связи с чем актуальны поиск и разработка дополнительных идей, методов, технологий, привлечение к решению проблемы дополнительных компетенций из смежных областей знаний.
2. Цель работы, решаемые задачи
Выносимые на обсуждение базовые целевые требования и критерии, которые могут быть полезны для налаживания междисциплинарного взаимодействия при совершенствовании имеющихся методов и средств воздействия на ход эпидемиологических процессов (ЭП) и разработке новых, формулируются следующим образом:
- Безопасность. Коллективная и персональная.
- Положительная эффективность при выполнении требований п. 1.
- Своевременность. Технологическая, организационная и экономическая доступность на момент востребования.
- Этическая приемлемость для социумов.
Характеристики известных методов купирования эпидемий и пандемий соответствуют приведённым критериям, к сожалению, лишь частично. Расхождения наблюдаются главным образом относительно пунктов 1, 3, в некоторых случаях, пункта 4.
Один из возможных путей развития направления видится в привлечении к решению проблемы усовершенствованных, не затрагивающих метаболизм защищаемых организмов, методов прямых, ограниченных в целях гарантии безопасности рамками действующих санитарных правил и норм (СанПиН), volatile organic compounds (VOC), физико-химических воздействий на патогенные микроорганизмы. При этом патогенные микроорганизмы рассматриваются как наноразмерные (с отношением площади поверхности к объёму 1,0*10Е6 и более) физические тела содержащие белковые структуры, подлежащие видоизменению или деструкции, в первую очередь, расположенные на поверхностях микроорганизмов, отвечающие за механизмы инвазии. Расширенное использование с указанной целью появившихся и вошедших в практику технологий и поддерживающих их технических средств в областях физики, химии, электрохимии, электроники, IT-технологий, методов и средств математического моделирования, систем обработки больших баз данных.
Применённые в представленной работе компетенции в значительной части являются и поддерживаются «электронными» технологиями [1] вследствие чего имеют возможность в качестве исполнительных консолей комплиментарно встраиваться и дополнять состав имеющихся и разрабатываемых национальных и межнациональных автоматических медицинских real-time систем мониторинга эпидемиологического благополучия социумов,
3. Идея метода
Рассматривая стадии и ход ЭП [2, с. 54-55] вызываемого заразным началом передающимся воздушно-капельным путём, возможно сделать уточнение – фактическим, на уровне морфологии, источником сообщающим в окружающую среду заразное начало (эмитентом), равно как и воспринимающим его организмом (акцептором), являются не организмы в целом как таковые, а лишь их конкретные ткани, а именно поверхности слизистых оболочек (органов дыхания, зрения, пищеварения) зараженного и заражаемого организмов. При этом, для поддержания жизненного цикла, патогенный микроорганизм неминуемо должен дважды преодолеть четко и однозначно локализованный барьер: поверхность слизистых – окружающая среда при эмиссии и окружающая среда – поверхность слизистых при акцепции. Размещение и поддержание на поверхности слизистых оболочек в местах возможного заражения членов социума субстанций, препятствующих прохождению патогенов через указанный барьер и влияющих на их способность к инвазии, репликации и распространению, по мнению автора имеющего длительный инженерный опыт работы в соответствующих прикладных областях, к настоящему времени является технически, организационно и экономически доступной технологией и может быть материальной основой для дополнительного к существующим либо самостоятельным методом профилактики, контроля распространения и прекращения ЭП.
Подтверждением тезиса может служить имеющаяся успешная по отношению к некоторым инфекциям практика применения метода вакцинации. Превентивно активированная иммунная система организмов непрерывно вырабатывает, поддерживает и регулирует, в том числе на поверхностях слизистых, противодействующие инфекции вещества - антитела. Выработка противодействующего вещества собственным метаболизмом организма обеспечивает биологическую совместимость вещества с тканями, что определяет возможность, пусть и не большого в количественном отношении, но превентивного присутствия в нужное время и нужном месте противодействующего инфекции фактора. Как следствие, результатом наблюдаются повышенная специфическая устойчивость организмов к патогену, безопасность, своевременность и эффективность защиты от внезапных патогенных атак.
Одной из целей работы являлся поиск и исследование субстанций пригодных для длительного, соизмеримого с длительностью ЭП, диспергирования в воздух защищаемых пространств и, в отличие от известных антисептиков и дезинфектантов, допускающих, подобно антителам, безопасное пролонгированное присутствие на поверхностях слизистых и способных выполнять на физико-химическом уровне некоторые функции антител, не проникая при этом своим действующим началом в ткани организма и не взаимодействуя с его метаболизмом.
4. Патопротекторы
Субстанции рассматриваемого целевого назначения, обладающие комплексом свойств, удовлетворяющих изложенным выше критериям п. 1, п. 2, п. 3 и возможных к массовому применению в периоды эпидемиологических угроз, рационально выделить в отдельную группу веществ. Предлагаемое название группы - патопротекторы (pathoprotector) (от лат. мед. patho- «болезнь» и protecto – «защищать»). В качестве основных параметров классификации групп патопротекторов, по аналогии с методикой определения индекса селективности лекарственных средств, можно предложить:
- На качественном уровне – параметры, характеризующие спектр действия относительно видов подавляемых патогенных микроорганизмов и видов защищаемых организмов.
- На количественном уровне – достигаемый интегральный индекс селективности действия (ИИСД), определяемый как отношение значений достигаемой противоэпидемиологической эффективности к значениям параметров, характеризующих изменение индекса здоровья социума, вызываемого применением технологии.
Образно можно сказать, что идея создания веществ-патопротекторов, диспергируемых в местах возможного распространения ЭП, это идея создания «одежды для слизистых». Аналогично термопротекторам (знакомой всем одежды), искусственных оболочек защищающих организмы людей от неблагоприятных факторов окружающей среды отличным от принятого в природе образом.
4.1. Патопротекторы на базе ион-металлических водных композитов
Основной сложностью и сомнением для специалистов в возможности реализации предлагаемого метода следует считать создание субстанций, сбалансированных по параметрам безопасность – эффективность – стоимость на уровне, позволяющем массовое применение в периоды эпидемиологической опасности. При этом вопрос безопасности субстанций подлежит рассмотрению с особой тщательностью поскольку метод подразумевает воздействие случайным образом на любого участника ЭП вне зависимости от его персональных особенностей (возраст, пол, состояние здоровья, склонность к аллергическим реакциям, индивидуальная непереносимость препаратов, иных органических и не органических веществ).
Закономерен вопрос – возможно ли и каким образом, с использованием каких принципов действия, создание веществ с указанным комплексом свойств при имеющемся уровне знаний и развития технологий?
Одним из действующих начал патопротекторов, по крайней мере по отношению к некоторым видам респираторных вирусных инфекций, по мнению автора, могут быть ион-металлические водные композиты (ИМВК). Синтезируемые особым образом простые неорганические вещества неспецифического действия. Химический состав ИМВК принципиально и целенаправленно лаконичен. Содержит лишь две вещественные компоненты, совмещаемые физическими методами; воду выполняющую роль растворителя (предпочтительно высокого уровня чистоты, с минимальным содержанием сторонних примесей) и металл, один или в сочетании из нескольких, присутствующий в растворе в активной ионной (катионной) форме.
Следует сразу отметить, что, известные, традиционно именуемые и воспринимаемые специалистами как ионные, известные водные растворы металлов получаемые химическими способами, например путём растворения солей, а также растворы с дополнительными веществами вводимыми в состав в целях стабилизации действующего начала растворов, для использования в качестве патопротекторов не пригодны по критерию «безопасность» из-за присутствия в субстанциях в значимых количествах сторонних водорастворимых веществ, обладающих токсикологическим и сенсобилизирующим профилями, иногда значительными, например, анионные солевые остатки, поверхностно-активные вещества (ПАВ), кислоты, щелочи, иные органические и не органические вещества, способные, будучи водорастворимыми, по законам осмоса, мигрировать в ткани организма нарушая их нормальное функционирование, особенно при длительном воздействии.
Наиболее близкими по биологическим свойствам к ИМВК, возможными в экстренных случаях, в ограниченных дозировках, к применению в качестве патопротекторов, являются известные «классические» водные растворы металлов, получаемых методом электролитического растворения в слабо минерализованных водных растворах, например растворы ионного серебра в питьевой воде [3, с. 54-55]. Возможные ограничения их применения для рассматриваемых целей связаны с сопутствующим процессу электролиза неизбежным появлением в растворах дополнительных сторонних токсичных составляющих в количествах соизмеримых с количеством целевого металла которые образуются в следствии попутно происходящих побочных окислительно-восстановительных реакций, трансформации электролито-образующих веществ под действием проходящего через электролит электрического тока.
Для выполнения экспериментальных апробаций воздействия предлагаемой технологии на ход эпидемиологических процессов в работе применялись две модификации монометаллического ИМВК, производимых в лаборатории компании ООО «Нью Лайн» г. Санкт-Петербург, с текущими лабораторными технологическими обозначениями ВАХ-50 и Вах-100 в которых используется металл серебро как наиболее изученный и имеющий обширную базу данных в части биологического действия. Субстанция ВАХ-50 бюджетный препарат общего применения с ограниченным (до 3-х суток) сроком годности, приготавливается ex temporo с использованием серебра промышленной марки Ср 99,9 по ГОСТ 6836-2002 и дистиллированной (деминерализованным методом обратного осмоса) воды по ГОСТ Р 6709-72 с фактическим остаточным уровнем минерализации и фоновых примесей 3,5 ± 0,5 мг/дм3. Препарат ВАХ-100 особо чистый, с увеличенным сроком годности (3 месяца), выполняется с применением дополнительной финишной технологической стадии физической ион-гидратной стабилизации. Приготавливается с использованием серебра промышленной марки Ср 99,99 по ГОСТ 6836–2002 и деионизированной воды, соответствующей стандартам ОСТ 11.029.003-80 и ASTMD-5127-90 с фактическим остаточным уровнем минерализации и фоновых примесей не более 0,05 мг/дм3.
Значения кислотности обоих препаратов находятся в области близкой нейтральной (типовое значение pH = 7,1±0,6). Содержание металла серебро в растворах одинаково и составляет 20±3,0 мг/дм3.
За вычетом незначительного количества сторонних примесей препараты ИМВК ВАХ-50 и ВАХ-100 допустимо рассматривать как вещества состав которых формируется лишь тремя химическими элементами; водород, кислород и металл (серебро). Форма присутствия в растворах металла серебро в настоящий момент детально не изучена. Помимо надёжно фиксируемой преобладающей ионной (катионной) формы возможно предположить присутствие некоторых количеств металла в форме гидратов, оксидов и наноколлоидов.
В ходе технологических изысканий по теме ИМВК выявлено существенное влияние даже малых количеств сторонних примесей на физико-химические свойства, временную стабильность и биоактивность ИМВК. Высокая чувствительность свойств препаратов к количеству содержащихся в них сторонних примесей хорошо проявляется на спектрограммах поглощения растворов (диапазон 200–800 nm). На рисунке 1 приведены спектрограммы поглощения а) препарата ВАХ-50 с содержанием примесей 3,5 мг/дм3 и б) ВАХ-100 с содержанием сторонних примесей 0,05 мг/дм3.
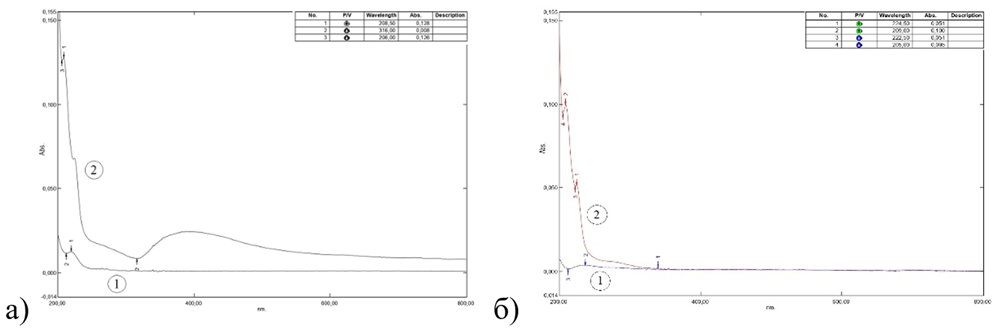
Рис. 1. Спектрограммы поглощения препаратов а) ВАХ-50, б) ВАХ-100, где; 1 – вещество сравнения вода деионизированная, 2 – исследуемый раствор
Органолептически ВАХ-100 определяется как бесцветная прозрачная жидкость, у ВАХ-50 возможно заметить проявления цветности и опалесценции. Обе субстанции без запаха (0 баллов), ощутим металлический привкус (3 балла). При этом ВАХ-100 характеризуется значительно большим (более чем на порядок) временем стабильного существования раствора, под которым понимается время от изготовления до начала заметного ускорения процесса перехода металла из потенциально не устойчивой ионной в более устойчивую коллоидную форму, которая классифицируется в рассматриваемом контексте как сторонняя примесь. Также у химически более чистого препарата ВАХ-100 наблюдается несколько большая (в среднем на 10–30%) активность по отношению к патогенным микроорганизмам.
По отношению к организму человека при местном применении токсического действия, сенсибилизирующих эффектов в пределах чувствительности методов по ГОСТ33483-2015 препараты ВАХ-50 и ВАХ-100 не проявляют (0 баллов). Более глубоких токсикологических исследований к настоящему времени не проводилось. Однако, к аргументам в пользу предполагаемого достаточного для рассматриваемых целей, уровня безопасности ИМВК можно отнести долговременную (с 1996 г. по настоящее время) практику клинического применения в целях профилактики инфекционных осложнений, снижения интенсивности воспалительных (аутоиммунных) процессов, ускорения заживления, препятствования образованию спаек и гипергрануляции регенерируемых тканей в отделениях инфекционной хирургии г. Санкт-Петербурга ионн-серебрянного препарата местного применения ВАХ-25 [4, с. 98]. ВАХ-25 препарат предшествующего технологического поколения ИМВК, химически менее чистый, получаемый классическим способом электролиза in temporo в клинике на оборудовании выполненном согласно патентным источникам [5, 6] с использованием мало минерализованной питьевой воды с уровнем естественной минерализации в пределах 80–120 мг/дм3. За более чем 25 лет и более 20-ти тысяч наблюдений случаев возникновения побочных эффектов не отмечено. Данное клиническое наблюдение явилось основной предпосылкой развития темы ИМВК и идеи создания патопротекторов на их основе.
Основным механизмом действия ИМВК на биологические объекты считается способность катионов металлов вступать в связь с белками, что искажает структуру белков, способствует процессам их коагуляции и иным видоизменениям, приводящим к нарушению и пассивации функционала белковых структур и, как следствие, микроорганизмов в состав которых они входят [7, с. 45-47]. При падении капли аэрозоля на гидрофильную поверхность слизистых происходит растекание препарата по поверхности тонким слоем, в пределе до мономолекулярного, с большой площадью покрытия. При этом компонент препаратов способный проникать вглубь тканей – вода, является веществом глобально совместимым с тканями организма. Действующее начало препаратов – металл в ионной форме, активно взаимодействует и связывается с органикой, содержащейся на поверхности и в толще слизистых выделений. В связанном виде ион металла теряет подвижность и способность мигрировать вглубь тканей. В дальнейшем, не накапливаясь, под действием процессов естественной регенерации слизистых, работы мукоцилиарной системы, выводится из органов и удаляется из организма.
4.2. Экспериментальная оценка бактерицидной активности ИМВК in vitro
Несмотря на лаконичность химического состава, препараты ИМВК показывают стабильные антисептические свойства, оцениваемые как достаточные для рассматриваемого приложения. Ниже в таблицах 1, 2 представлены типичные результаты скрининговых микробиологических определений препарата ВАХ-100 по отношению к референтным и «диким» резистентным штаммам актуальных внутрибольничных инфекций (на примере актуальных штаммов 2021–2022 г. из коллекции НИИЭМ им. Пастера, г. Санкт-Петербург).
Исследования антибактериального действия препарата производились путём высева после совместной инкубации микроорганизмов с препаратом. Для этого на физиологическом растворе готовили взвесь суточных культур микроорганизмов в концентрации 1·105 м.к./мл, вносили инокулюм каждого микроорганизма в лунки планшета по 100 мкл, добавляли в них по 10 мкл исследуемого препарата. Опыт сопровождали контролями для каждой культуры, где вместо препарата в инокулюм добавляли по 10 мкл стерильной дистиллированной воды. После 18 часов инкубации при температуре +37оС из каждой лунки производили высев по 10 мкл на плотные питательные среды. На следующий день подсчитывали количество выросших колоний на каждой чашке, соответствующей одной лунке планшета. Все эксперименты проводили в трех повторностях. Далее рассчитывали среднее арифметическое для каждой позиции (табл. 1, 2).
Таблица 1
Результаты исследования антибактериального действия препарата ВАХ-100 в отношении референтных штаммов
Наименование микроорганизма | Количество выросших бактерий | |
Без использования препарата (контроль) | С использованием препарата ВАХ-100 | |
P. aeruginosa ATCC 27853 | 5×104 | 2×101 |
K. pneumoniae ATCC 13883 | 6×104 | 0 |
S. aureus ATCC 25923 | 4×104 | 0 |
E. coli ATCC 25922 | 5×104 | 0 |
A. baumannii ATCC 17978 | 3×104 | 7×101 |
C. albicans ATCC 10231 | 6×103 | 0 |
Таблица 2
Результаты исследования антибактериального действия препарата ВАХ-100 в отношении «диких» резистентных штаммов внутрибольничных инфекций
Наименование микроорганизма | Количество выросших бактерий | |
Без использования препарата (контроль) | С использованием препарата на основе серебра ВАХ-100 | |
P. aeruginosa | 5×104 | 5×102 |
K. pneumoniae | 2×104 | 0 |
S. aureus | 3×104 | 0 |
E. coli | 3×104 | 0 |
A. baumannii | 2×104 | 0 |
C. albicans | 4×103 | 2×101 |
Во всех определениях in vitro у исследовавшихся в ходе работ штаммов микроорганизмов, грамположительных, грамотрицательных, грибков, стабильно отмечалось наличие чувствительности к ИМВК, в некоторых случаях значительной, на уровне более характерном для дезинфектантов. Также интересна прослеживающаяся общая взаимосвязь чувствительности исследуемых видов микроорганизмов к препаратам ИМВК в зависимости от их геометрических размеров и плотности присутствия на их поверхностях (включая жгутики, пилии, шипы) биологически активных белковых структур. При уменьшении физических размеров (увеличении отношения площади поверхности к объёму микроорганизма) наблюдается общая тенденция к росту эффективности действия ИМВК.
4.3. Экспериментальная оценка вирулицидной активности ИМВК in vitro
Целью исследования было изучение противовирусных свойств растворов ИМВК в отношении оболочечных вирусов человека на примере вируса гриппа А (H1N1).
4.3.1. Материалы и методы. Реактивы и приборы
Вирус гриппа A/Puerto Rico/8/34 (H1N1), исходный титр 5×106 TCID50/мл.
Культура клеток MDCK, почка собаки (ATCC; Кат. № CCL-34);
Полная (ростовая) среда MEM (Gibco, UK, Cat.#22561), содержащая 2 mM L-глутамина, 250 мг/л гентамицина, 10% эмбриональной сыворотки крупного рогатого скота (Gibco, Бразилия, Cat.#10270);
Поддерживающая среда MEM (Gibco, UK, Cat.#22561), содержащая 2 mM L-глутамина, 250 мг/л гентамицина, 2 мкг/мл трипсина;
Физиологический раствор (0.9% раствор NaCl в дистиллированной воде, стерильный, компания «Биолот», Санкт-Петербург, Кат. № 1.2.1.3); флаконы для клеточных культур 25 мл (Corning, США); 96-луночные планшеты (Corning, США, Кат. № 3585); наконечники для автоматических пипеток 20–200 мкл; ламинарный бокс, второго класса защиты (БОВ-001-АМС, Миасс, Россия); CO2- инкубатор MCO-175 (Panasonic, Япония);
4.3.2. Дизайн исследования
Клетки MDCK сеяли во флаконы для клеточных культур или в 96-луночные планшеты и инкубировали 24 часа в атмосфере 5% CO2 при 36°С до формирования монослоя. Вирус наращивали в монослое клеток во флаконах для клеточных культур в течение 48 ч при 36°С.
В исследовании использовали образцы водных растворов содержащие ионы серебра меди или их комбинацию. Всего было изучено 4 образца: три раствора получаемых «классическим» электролитическим способом на основе слабоминерализованной (100±20 мг/дм3) питьевой воды; 1 – Ag (ВАХ-25), 2 – Cu, 3 – Ag+Cu (½+½) и 4 – препарат ИМВК ВАХ-50 получаемый на основе дистиллированной воды. Содержание металла во всех препаратах составляло 20±2,0 мг/дм3.
Препараты разводили физиологическим раствором (0,9% NaCl) в соотношении 1:2, соответственно, с концентрацией металла в рабочих растворах 10,0±2,0 мг/дм3. В качестве препарата сравнения использовался коммерческий препарат протеината серебра (протаргол), который разводили в 6 раз.
Раствор протаргола содержит 2% протеината серебра, в котором на долю серебра приходится 8%, или 160 мг/дм3. Таким образом, разведение 2%-го раствора протаргола в 6 раз дает концентрацию металла серебра в рабочем растворе 27 мг/дм3, что сопоставимо с концентрацией металла в рабочих растворах ион-металлических композиций 10 мг/дм3.
Первая серия экспериментов была направлена на оценку вирулицидной активности препаратов. К изучаемым растворам добавляли вирус гриппа в соотношении 9:1 (об./об.) и инкубировали полученные смеси в течение 30 минут при 37°С. По истечении этого срока в вируссодержащей жидкости определяли инфекционную активность вируса как описано ниже. В каждой группе образцов использовали четыре параллели.
Вторая группа экспериментов была направлена на изучение воздействия препаратов на способность клеток в культуре поддерживать репродукцию вируса в условиях предварительной инкубации. Для этого изучаемые растворы вносили в лунки планшетов с клетками, инкубировали в течение 30 минут при 37°С в атмосфере 5% CO2, после чего препараты отмывали средой МЕМ. К клеткам добавляли вирус гриппа из расчета 1 TCID50 на 10 клеток (m.o.i. 0.1), инкубировали в течение 1 часа при 37°С в атмосфере 5% CO2, после чего не связавшийся вирус отмывали средой МЕМ. Планшеты с клетками инкубировали в течение 72 часов при 37°С в атмосфере 5% CO2, после чего наличие вируса в лунках определяли при помощи реакции гемагглютинации (см. далее). В каждой группе образцов использовали четыре параллели.
4.3.3. Титрование вируса
Из исследуемой вируссодержащей жидкости готовили серию 10 кратных разведений (10-1–10-7) на среде MEM. Этими разведениями заражали клетки культуры и инкубировали в термостате в течение 72 часов. По окончании срока инкубации наличие вируса в лунках определяли при помощи реакции гемагглютинации (см. далее).
4.3.4. Реакция гемагглютинации (РГА)
Для определения наличия вируса гриппа в культуральной жидкости проводили реакцию гемагглютинации. Для этого культуральную жидкость переносили в лунки планшета для иммунологических реакций, после чего добавляли равный объем 1% куриных эритроцитов в физиологическом растворе. Планшеты инкубировали при 20°С в течение 1 ч, после чего визуально проводили учет результатов. За титр вируса принимали наибольше разведение вируссодержащего материала, при котором наблюдалась положительная реакция гемагглютинации. Положительным считают результат реакции, при котором эритроциты равномерно покрывали всё дно лунки. При отрицательной реакции эритроциты в виде маленького диска или «пуговки» располагаются в центре дна анализируемой лунки планшета.
4.3.5. Статистическая обработка результатов
Результаты измерения инфекционного титра вирусов представляли в виде M±SE, где M – среднее значение, SE – ошибка эксперимента. Полученные данные сравнивали между собой в парах «вирус после инкубации – вирус без инкубации» с помощью критерия Стьюдента. Различия считали значимыми при р < 0,05.
4.4. Результаты исследования
Результаты определения инфекционного титра вируса гриппа до и после инкубации с изучаемыми образцами ион-металлических водных композитов суммированы в таблице 3 и для наглядности представлены на рисунке 2.
Таблица 3
Влияние инкубации с образцами ион-металлических водных композитов на инфекционную активность вируса гриппа A/Puerto Rico/8/34 (H1N1). Исходный титр вируса – 6,0 lg TCID50/0.2 мл
Инфекционный титр вируса гриппа (lg TCID50/0.2 мл) после инкубации с образцом | |||||
Ag (ВАХ-25) | Cu | Ag+Cu | BAX-50 | Протаргол | Контроль вируса |
4,5±0,6 (16%) (p=0.098) | 5.0±0.0 (50%) (p=0.391) | 4.5±0.6 (16%) (p=0.098) | 4.0±0.0 (5%) (p=0.015) | 4.3±0.5 (10%) (p=0.030) | 5.3±0.5 (100%) |
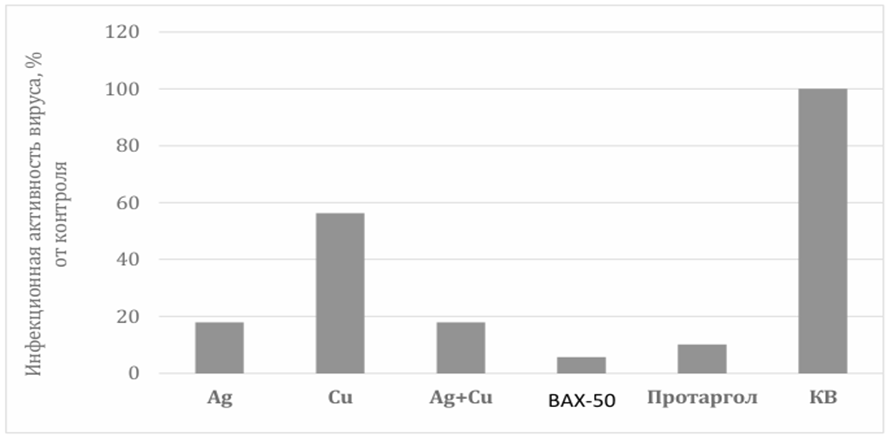
Рис. 2. Вирулицидные свойства ион-металлических водных композитов в отношении вируса гриппа A/Puerto Rico/8/34 (H1N1)
Как видно из представленных результатов, инкубация вируса с растворами ион-металлических водных композитов приводила к потере инфекционной активности вируса. Наибольшей активностью обладал образец BAX-50, при использовании которого различия в титрах исходного и конечного образцов вируса составила 1,3 порядка, что соответствует снижению вирусной активности на 95%. Полученные данные свидетельствуют, что вирулицидная активность изученных образцов обусловлена преимущественно ионами серебра, поскольку лишь в этих образцах отмечалось снижение вирусного титра, пусть и не всегда до достоверных величин. Образец «Cu» приводил к потере вирусом инфекционных свойств в наименьшей степени, и различия не достигали достоверных значений.
Вторая группа экспериментов была направлена на изучение влияния ИМВК на клеточные рецепторы, связывание с которыми является первым и необходимым условием реализации жизненного цикла вируса. Для этого клетки были обработаны изучаемыми растворами, после чего была изучена способность вируса гриппа размножаться в такой культуре. Результаты исследования суммированы в таблице 4 и для наглядности представлены на рисунке 3.
Таблица 4
Влияние предварительной инкубации клеток MDCK с образцами ион-металлических водных композитов на инфекционную активность вируса гриппа A/Puerto Rico/8/34 (H1N1). Исходный титр вируса – 6,0 lg TCID50/0.2 мл
Инфекционный титр вируса гриппа (lg TCID50/0.2 мл) после инкубации культуры клеток с препаратами | |||||
Ag (ВАХ-25) | Cu | Ag+Cu | BAX-50 | Протаргол | Контроль вируса (КВ) |
5.5±0,6 (32%) (p=0.182) | 6.0±0.5 (100%) (p=1.000) | 5.8±0.5 (63%) (p=0.391) | 5.5±0,6 (32%) (p=0.182) | 5.3±0.5 (20%) (p=0.058) | 6.0±0.0 (100%) |
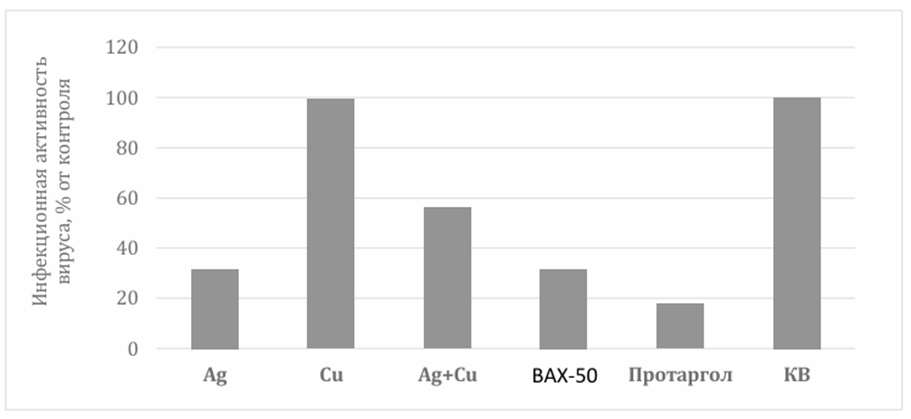
Рис. 3. Влияние ион-металлических водных композитов на способность клеток MDCK поддерживать репродукцию вируса гриппа A/Puerto Rico/8/34 (H1N1)
Как следует из представленных данных, ни один из изученных образцов не приводил к достоверному снижению вирусной активности при условии предварительной обработки клеток. Наибольшую эффективность проявил препарат сравнения – протаргол, что можно объяснить наличием в его составе белкового компонента, способного неспецифически связываться с рецепторами на поверхности клетки. Различия в титрах вируса, однако, и в этом случае не достигали достоверных величин (p = 0.058).
Таким образом, изученные ИМВК проявили способность к умеренной вирулицидной активности, снижая в оптимальном случае титр вируса гриппа за 30 минут инкубации на 1,3 порядка, что соответствует снижению вирусной активности на 95%.
5. Интегральный индекс селективности действия технологии
При выполнении условия обеспечения безопасности эффективность метода и технологии может регулироваться в широких пределах за счёт изменения интенсивности применения. В связи с чем, возможность достижения высоких предельных значений ИИСД допустимо рассматривать как результат достижения высоких показателей безопасности технологии, которые определяются использованием трёх взаимодополняющих и страхующих факторов:
- Системный фактор в виде соблюдения законодательно закреплённых правил и норм безопасности факторов окружающей среды для здоровья человека (СанПиН, VOC), в том числе с учётом возможных синергетических явлений.
- Физико-химический фактор. Применение субстанций потенциально токсичная компонента которых ограничена в возможности проникать в ткани организма и взаимодействовать с его метаболизмом по физико-химическим причинам.
- Биохимический фактор. Применение субстанций действующее начало которых характеризуется высокими показателями индекса селективности.
В настоящий момент объём и глубина выполненных исследований не достаточны для достоверных оценок возможных к достижению значений ИИСД метода. Наименее исследованными являются группы явлений, касающихся 1-го и 2-го фактора безопасности. Одной из особенностей предложенной технологии, позволяющей привлекать и задействовать в более полном объёме фундаментальную сумму знаний, накопленную и выраженную в виде СанПиН, VOC, является предположение, что относительно малое по абсолютным значениям, но продолжительное по времени воздействие патопротекторов на патогенные микроорганизмы могут оказывать существенное влияние на ход ЭП, его последствия.
Необходимость проверки тезиса была учтена при формировании дизайна экспериментов с использованием биологических моделей.
Учитывая наличие у паторотекторов отличного от классического, двойного механизма обеспечения безопасности (п. 2, п. 3 факторов), влияющего на их биосовместимость, типовых определений по стандартным методикам индекса селективности ИМВК in vitro на текущем этапе работ не проводилось, возможность и корректность использования стандартного показателя не оценивалась. Выбор наиболее перспективных вариантов ИМВК для выполнения экспериментов in vivo выполнялся на основании локального, ограниченного рамками выполненных определений, коэффициента асимметрии действия (КАД) препаратов в опыте на основании данных, полученных при определении вирулицидной активности препаратов in vitro.
При определении КАД были приняты следующие допущения:
- Снижение инфекционной активности вируса в следствие воздействия рабочих растворов препаратов является желаемым положительным результатом.
- Снижение возможности культуры поддерживать репликацию вируса в следствии воздействия препаратов на культуру клеток MDCK рассматривается как нежелательное, отрицательное воздействие препаратов на уровень метаболической активности, «здоровье» культуры клеток.
С учётом допущений, возможно определить значение КАД препаратов в опыте воспользовавшись следующим соотношением:
КАДₓₙ = К⁺ₓₙ / К⁻ₓₙ, (1)
Где, К⁺ₓₙ, К⁻ₓₙ коэффициенты положительного и отрицательного воздействия препарата xn, определяемых как отношение инфекционного титра контроля вируса принимаемого за 100% к выраженному в процентах значению инфекционного титра патогена в текущей серии определений, то есть:
К⁺ₓₙ = 100 % / ИТ⁺ₓₙ (%), К⁻ₓₙ = 100 % / ИТ⁻ₓₙ (%), (2).
Применяя соотношения (2) и (1), определяются значения КАД препаратов в эксперименте. Результаты приведены в таблице 5 и для наглядности представлены на рисунке 4.
Таблица 5
Результаты определения значения коэффициента асимметрии действия препаратов в эксперименте
| Значения КАД рабочих растворов препаратов | |||||
Коэффициенты | Ag (ВАХ-25) | Cu | Ag+Cu | BAX-50 | Протаргол | Контроль вируса |
К⁺ | 6,25 | 2,0 | 6,25 | 20,0 | 10,0 | 1,0 |
К⁻ | 3,12 | 1,0 | 1,58 | 3,12 | 5,0 | 1,0 |
КАД | 2,03 | 2,0 | 3,95 | 6,41 | 2,0 | 1,0 |
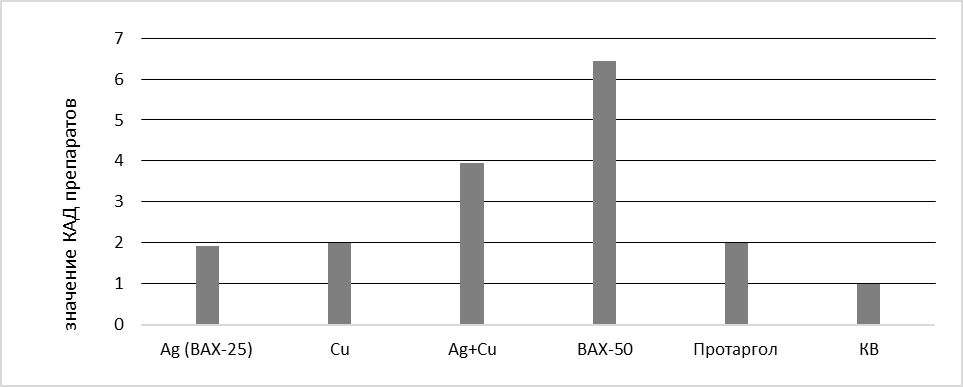
Рис. 4. Значения коэффициента асимметрии действия препаратов в опыте
На основании данных таблицы 5 можно констатировать, что препарат ВАХ-50 характеризуется существенно большей асимметрией действия по отношению к патогенному микроорганизму и клеточной культуре чем иные исследованные препараты, соответственно, является более перспективным в дальнейших экспериментах in vivo в качестве вещества-патопротектора.
6. Экспериментальное определение in vivo параметров эффективности и безопасности патопротекторов на основе ИМВК при групповой аэрозольной технологии применения
Общее. Наиболее проблемным моментом при экспериментальном моделировании ЭП in vivo вызываемого инфекциями, распространяющимися воздушно-капельным путём следует признать сложности с обеспечением стабильности, повторяемости и верификации параметров среды и путей распространения инфекции, их дальнейшее вычленение и учёт при обработке и интерпретации результатов исследований. В связи с чем, а также учитывая, что эксперимент рассматриваемой целевой направленности проводился впервые, для проверки состоятельности концепции, работоспособности метода и технологии, модельной средой распространения ЭП была выбрана поверхность лёгочной ткани млекопитающих. Выбор обоснован следующим:
- При выбранном варианте инфекция передаётся от пораженного участка ткани к здоровому фактически минуя стадию ЭП «пути распространения». В связи с чем возможно считать, что ослабление инфекции на путях миграции во внешней среде отсутствует и значение коэффициента изменения активности инфекции на путях миграции заведомо известно и равно значению 1,0 [8].
- Морфологически лёгкие являются органом, представляющим собою, упрощённо, тонкую компактно упакованную плёнку с очень большой площадью поверхности и очень малой толщиной. С точки зрения геометрии это двумерный объект, в котором, из-за малости его толщины, инфекция имеет возможность распространятся от точки первичного заражения преимущественно лишь по поверхности. При указанных геометрических условиях уровень эмиссии в окружающую среду размножившейся инфекции поддерживающей ЭП линейно связан с площадью поражения ткани. Площадь поражения пропорциональна наблюдаемому в объёме поражению лёгких, что является прямым, доступным для количественных определений, показателем уровня активности инфекции и влияния на него противодействующего фактора.
Более половины ресурсов эксперимента были выделены на выявление возможных побочных эффектов и ограничений верхних значений рабочих параметров интенсивности применения технологии. В качестве биологической модели выбраны мыши. Мыши обладают свойством реагировать на не благоприятные воздействия любой природы (химического, физического, социального, эмоционального) изменением динамики приращения массы тела.
Моделью заразного начала выбран возбудитель пандемии 2009 г. вирус гриппа A/Puerto Rico/8/34 H1N1 (свиной грипп). Патоген хорошо изучен, по-прежнему актуален, отличается высоким уровнем суточной репликации в лёгочных тканях, способностью оставлять в них надёжно определяемые карнификационные следы воздействия.
Исследование проводилось на методической и лабораторной базе НИИ эпидемиологии и микробиологии им. Пастера, г. Санкт-Петербург, вирусологическое отделение.
6.1. Описание эксперимента
Введение. Задачей исследования явилось изучение эффективности применения непрерывно генерируемого и поддерживаемого в ходе эксперимента защитного аэрозольного облака на базе ИМВК как средства профилактики и лечения гриппозной инфекции у лабораторных животных. В задачи работы входило моделирование нелетальной гриппозной инфекции у белых мышей, а также оценка протективной активности разработанных ООО «Нью-Лайн» г. Санкт-Петербург патопротекторов на основе ИМВК при аэрозольном применении методом формирования в контролируемом объёме постоянно действующих защитных аэрозольных облаков допускающих длительное безопасное пребывание на модели гриппозной пневмонии у животных.
Также оценивалась переносимость животными максимальных допустимых по технологии доз препаратов и производилась оценка переносимости экспериментальных сверхвысоких доз и порогов применимости технологии в целом.
6.2. Материалы и методы
6.2.1. Исследуемые препараты
В работе использовали препарат ИМВК ВАХ-50, разработанный компанией ООО «Нью-Лайн», г. Санкт-Петербург согласно рекомендованных методик применения, дозировок и технологических режимов работы предоставленного компанией оборудования (комплекта распылительных устройств – небулайзеров и вспомогательного оборудования).
6.2.2. Вирусы
В исследовании использовали вирус гриппа A/Puerto Rico/8/34 (H1N1) из коллекции вирусных штаммов НИИЭМ им. Пастера: Вирус накапливали в аллантоисной полости 8–10-дневных куриных эмбрионов и использовали в дальнейших экспериментах.
6.3.1. Дизайн исследования и регулирующие стандарты
Исследования выполняли в соответствии со следующими документами «Правила лабораторной практики в Российской Федерации» (Приказ Министерства здравоохранения Российской Федерации № 708н от 23.08.2010 г.) и «Руководство по проведению доклинических исследований лекарственных средств» Часть первая//под ред. А. Н. Миронова (2012). Исследования осуществляли согласно техническому заданию, утвержденному в договоре. Дизайн и организация исследования были направлены на решение поставленной цели и базировались на общих принципах проведения исследований по оценке противовирусной активности лекарственных препаратов.
6.3.2. Животные
Белых половозрелых мышей (самки) линии Balb/c массой 16–18 г (возраст 5-6 недель) получали из питомника «Рапполово» (Ленинградская область, Россия). Информация о группе эксперимента была размещена на передней поверхности клеток и включала дату начала эксперимента, дату инфицирования, название и режим введения изучаемого препарата.
6.3.3. Содержание животных
Животные содержались в стандартных условиях в соответствии с постановлением Главного государственного санитарного врача РФ от 29.08.2014 № 51 «Об утверждении СП 2.2.1.3218-14 «Санитарно-эпидемиологические требования к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)».
В период акклиматизации (5 дней) и эксперимента мыши были размещены в поликарбонатных клетках (BENEX а.с., Чешская Республика, тип Т3А, S=1200 см2) барьера открытого типа группами по 15 особей, на подстиле из опилок. Клетки покрыты стальными решетчатыми крышками с кормовым углублением. Площадь пола в клетке содержания для одного животного составила 80 см2 (минимально допустимая площадь 40 см2).
Корм для содержания лабораторных животных, рецепт № ПК-120-2_173ООО «Лабораторкорм» (Москва), приготовленный по ГОСТ Р 50258-92 в соответствии с нормами, утвержденными приказом МЗ СССР № 755 от 12.08.77 г., давали ad libitum в кормовое углубление стальной решетчатой крышки клетки. Животные получали воду, очищенную и нормированную по органолептическим свойствам, по показателям рН, сухого остатка, восстанавливающих веществ, диоксида углерода, нитратов и нитритов, аммиака, хлоридов, сульфатов, кальция и тяжелых металлов на основании ГОСТ 51232-98 «Вода питьевая. Общие требования к организации и методам контроля качества». Вода в стандартных поилках со стальными крышками-носиками, давалась ad libitum. В качестве подстила использовали древесные гранулы (ООО «ИП Кострюкова», Москва, Россия).
Микробиологический контроль подстила и воды не проводился.
Животные содержались в контролируемых условиях окружающей среды (согласно СанПин 20‑26°C и относительной влажности воздуха помещения в пределах 50–70%). Устанавливался режим вытяжной вентиляции, обеспечивающий уровень воздухообмена около 15 объемов помещения в час. Температура и влажность воздуха регистрировались ежедневно. Мыши содержались в условиях естественного освещения. Никаких существенных отклонений указанных параметров в период акклиматизации и в ходе эксперимента не произошло.
6.3.4. Карантин
Мыши были адаптированы в виварии в отдельной комнате в течение 5 дней до начала эксперимента. Во время этого периода осуществлялся ежедневный осмотр внешнего состояния животных и клинический осмотр до рандомизации.
В ходе осмотра не было обнаружено животных с отклонениями, не позволяющими включить их в эксперимент.
6.4. Эвтаназия
Эвтаназия (безболезненное умерщвление животного) производилось ответственным лицом в соответствии с требованиями, принятыми в институте, путем цервикальной дислокации. Эвтаназия осуществлялась своевременно по окончании экспериментов, без причинения страданий, в помещении, где не содержатся другие животные. Уборка трупов мышей производилась только после того, как смерть была констатирована ответственным лицом.
В случае преждевременной гибели животных производился их визуальный осмотр с определением возможных причин гибели.
6.5. Оценка протективной активности аэрозоля ион-металлических композитов в опытах in vivo
Лабораторных животных (белые мыши линии Balb/c, самки, возраст 6–8 недель) разделяли на 4 группы по 15 животных в группе. Животных содержали в атмосфере изучаемого аэрозоля в минимальной дозе соответствующей предполагаемой номинальной профилактической дозе при практической реализации технологии (группа 1), средней, соответствующей максимально возможной технологической, дозе (группа 2) и максимальной дозе соответствующей сверхвысокой экспериментальной для целей определения граничных условий применимости метода (группа 3). Животные контрольной группы (группа 0) содержались в стандартной атмосфере, без аэрозоля.
Через 2 суток после начала обработки непрерывно генерируемом небулайзерами аэрозолем мышей в группах 0, 1 и 3 заражали интраназально под легким эфирным наркозом вирусом в дозе 3×102 TCID50 на мышь в объеме 30 мкл. Обработку аэрозолем продолжали в течение 5 суток после инфицирования. Наблюдение за животными проводили в течение 14 дней. Ежедневно фиксировали вес и смертность животных в каждой группе опыта. На 15 сутки после заражения животных умерщвляли при помощи цервикальной дислокации, вскрывали и изолировали легкие. Визуально оценивали размер очагов постгриппозной пневмонии, который выражали в процентах от общей поверхности легких.
6.6. Статистическая обработка результатов
Полученные данные обрабатывали при помощи программы Microsoft Excel. Результаты представляли в виде M±SD. Сравнения между группами проводили при помощи критерия Стьюдента. Достоверными считали различия между группами, если параметр p не превышал 0,05.
6.7. Результаты исследования
6.7.1. Изучение динамики веса животных в ходе экспериментальной гриппозной пневмонии
Для оценки влияния аэрозоля ион-металлических композитов на динамику веса животных в ходе гриппозной инфекции был проведен мониторинг массы тела животных в течение 8 суток после инфицирования. Результаты суммированы и приведены на рисунке 5.
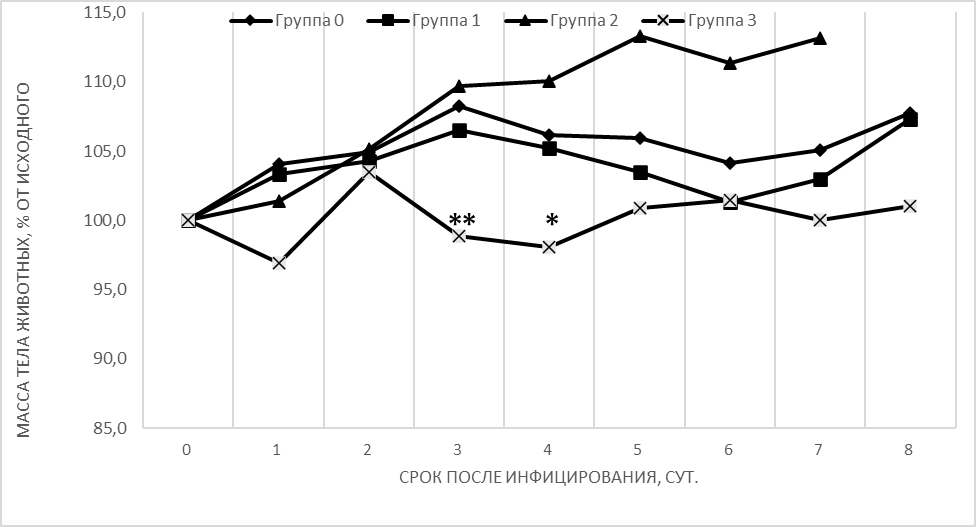
Рис. 5. Динамика массы тела белых мышей в ходе экспериментальной гриппозной пневмонии в условиях применения ион-металлических композитов. * p<0.05, ** - p<0.01
Как следует из представленных данных, находившиеся в аэрозольной атмосфере средней интенсивности интактные животные (группа 2) демонстрировали устойчивое нарастание массы тела в период 0–7 сутки после инфицирования. Заражение животных групп 0, 1, 3 вирусом гриппа в использованной дозе приводило к снижению весовых показателей, хотя отличия от контрольной группы не достигали достоверных величин. Постоянная обработка животных аэрозолем ион-металлических композитов не приводила к изменениям динамики массы, тогда как применение этого аэрозоля в экспериментальной сверхвысокой дозе отягощало течение инфекции, что проявлялось достоверным снижением массы мышей на 3 и 4 сутки после заражения.
6.7.2. Изучение влияния ион-металлических композитов на развитие постгриппозных поражений легких у животных
Как было показано в ходе визуального анализа легких животных, на 15 сутки после заражения в них развивались очаги хронической постгриппозной пневмонии, выглядевшие как участки карнификации легочной ткани (рис. 6). Доля поверхности легких, занятая такими участками, варьировала от 0 до 100%. Данные о среднем размере очагов пневмонии в экспериментальных группах суммированы в таблице 6.
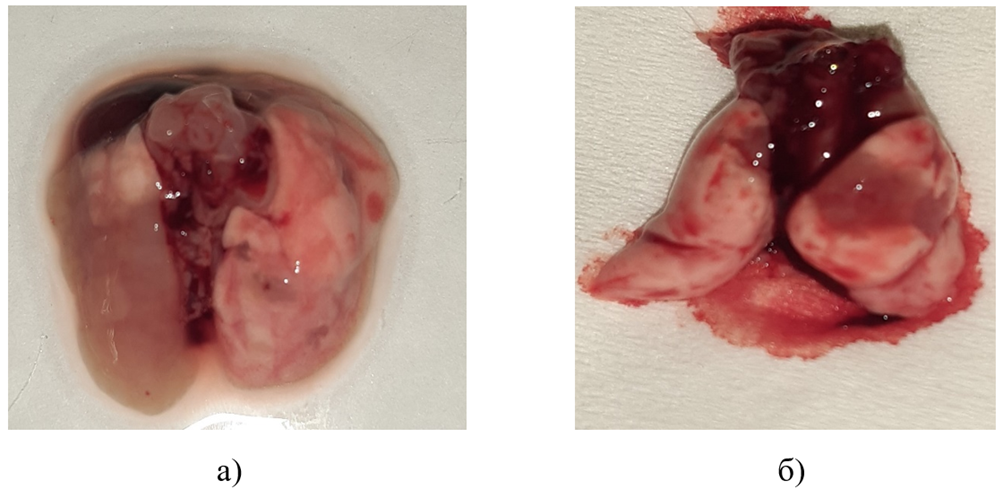
Рис. 6. Очаги хронической постгриппозной пневмонии в легких белых мышей на 15 сутки после заражения вирусом гриппа A/Puerto Rico/8/34 (H1N1). Ориентировочная площадь поражения 75% (а), 20% (б)
Таблица 6
Формирование очагов постгриппозной пневмонии в легких белых мышей на 15 сутки после заражения вирусом гриппа A/Puerto Rico/8/34 (H1N1) в условиях применения аэрозоля ион-металлических композитов
Группа опыта | Условия эксперимента | Средний размер очагов пневмонии, % | P |
0 | Зараженные животные без обработки аэрозолем | 28,3±5,1 | 1,000 |
1 | Зараженные животные, минимальная доза (предполагаемая базовая технологическая) обработки аэрозолем | 10,0±2,5 | 0,005 |
2 | Незараженные (интактные) животные, средняя (максимально достижимая технологическая) доза обработки аэрозолем | 0,0±0,0 | < 0,0001 |
3 | Зараженные животные, максимальная (сверхвысокая исследовательская) доза обработки аэрозолем | 24,2±7,6 | 0,667 |
6.8. Заключение
Проведено исследование протективных свойств аэрозоля ИМВК в экспериментах in vivo на модели экспериментальной гриппозной пневмонии у белых мышей, а также общая оценка граничных условий применения метода в области больших и сверхбольших концентраций аэрозоля.
Показано, что при средней (максимальной технологической) дозе аэрозоля в легких интактных животных не формируется визуальных патологических очагов поражений, вызываемых аэрозолем, а динамика изменения веса животных не имеет отклонений от типовой динамики изменения веса здоровых животных в нормальных условиях содержания. Побочных эффектов в рамках чувствительности методики эксперимента не выявлено.
Показано, что использование большой (экспериментальной сверхвысокой) дозы аэрозоля, приводящей к существенным изменением параметров среды обитания животных (постоянная влажность 100%), приводит к отягощению гриппозной инфекции. Это проявилось в гибели животных, достоверному снижению массы тела, а также отсутствию достоверных различий в степени поражения легких между этой группой и группой контроля.
В то же время установлено, что применение минимальной (предполагаемой базовой технологической) дозы аэрозоля приводит к достоверному снижению (в 2,8 раза) размеров очагов хронической постгриппозной пневмонии
В целом, полученные в эксперименте данные позволяют сделать следующие выводы на качественном уровне о предложенной к определению технологии:
- Обладает антивирусным действием в т. ч. на уровне нижних отделов дыхательной системы.
- Безопасна при длительном применении при соблюдении рекомендуемых дозировок.
7. Дополнительные сведения к эксперименту in vivo. Технические средства поддержки технологии
- Вывод об отсутствии изменений динамики веса животных от типовой сделан косвенным образом на основании справочных данных. Группа 2 интактных животных находившаяся под действием технологии показала за 7 суток среднее приращение веса особи в группе +2,3 грамма (0,32 грамма или 1,88% в сутки), что близко к максимальным известным значениям для мышей линии Balb/c, самки 7-8 недель. При воспроизведении экспериментов желательно предусматривать дополнительную контрольную интактную группу, не подверженную действию технологии.
- В группе 0, зараженных дозой вируса 3×102 TCID50 30 мкл на мышь и не обрабатывавшихся аэрозолем, наблюдались не типично низкий для применённой дозы процент поражения лёгких и динамика снижения веса. Причиной могла явиться не точность в расчетах при планировании эксперимента, прогнозируемой и полученной фактической, оказавшейся значительно большей, чувствительности инфекции к действию технологии. В дальнейшем рекомендуется принимать дополнительные меры по изоляции контрольных групп животных от возможного проникновения и влияния рассеянных частиц аэрозоля из соседних обрабатываемых групп.
Компоновка оборудования в помещении вивария. Представлена на рисунке 7.

Рис. 7. Компоновка экспериментального пространства и оборудования в эксперименте
В эксперименте лотки групп животных 0, 1, 2, 3 (рис. 7), располагались в ряд на средней полке лабораторного стеллажа. Небулайзеры групп 4.1, 4.2, 4.3 располагались на верхней полке стеллажа. Генерируемый аэрозольный поток из небулайзеров подавался в лотки по пластиковой гофрированной трубке (промрукав ПНД 20 DKC) диаметром 20 мм и длинной 900 мм. Небольшой диаметр подающих трубок и гофрированная поверхность способствовали удалению из потока возможных крупных не респирабельных фракций частиц аэрозоля и дополнительно стабилизировало работу небулайзеров по производительности. Аэрозоль поступал в лотки сверху в низ, выходное отверстие трубок располагались по центру клеток на высоте 300 мм над уровнем голов животных.
Для контроля параметров среды в лотках устанавливались датчики температуры и относительной влажности воздуха 8 (метеостанция Temeo Hygro Quadro 73257, BRESSER, Германия).
Под подстилкой 9 на дне лотков дополнительно располагались впитывающие возможный конденсат гидрофильные прокладки (памперсы) 10. Суточное изменение веса прокладок также являлось дополнительным параметром контроля среды обитания животных и стабильности работы оборудования.
Для разделения групп животных по воздушным потокам, защиты от беспокоящей засветки и сквозняков, лотки размещались в дополнительных пластиковых полуоткрытых боксах – ограждениях 7.
7.2. Небулайзеры, респирабельный состав частиц аэрозоля, дозы воздействия
В качестве небулайзеров использовались типичные увлажнители воздуха для жилых помещений «VITEK» VT-2341 производства Star Plus Limited, Hong Kong. Возможно применение любого другого подобного диспергирующего устройства использующего механический принцип распыления жидкости, например, оснащённых, как увлажнитель VT-2341 и аналогичные, типовыми ультразвуковыми дисковыми пезо активаторами (мембраной) диаметром 16–25 мм, рассчитанными на расход воды до 0,3–0,5 дм3/час. и электрической мощностью потребления 20–35 Вт [9]. Перед использованием увлажнители калибровались по производительности, проверялся дисперсный состав частиц генерируемого аэрозоля. Проверка дисперсности осуществлялась специализированным программно-аппаратным комплексом, прибором «Анализатор дисперсности атмосферных частиц SpectroPan Type-No 700800-PA-100, Германия» (ФГБУ НКЦТ им. Голикова ФМБА Россия, г. Санкт-Петербург, лаборатория токсикологии ИЦГО).
Гистограмма распределения торакального состава частиц аэрозоля, поступавшего в лотки групп представлена на рисунке 8.
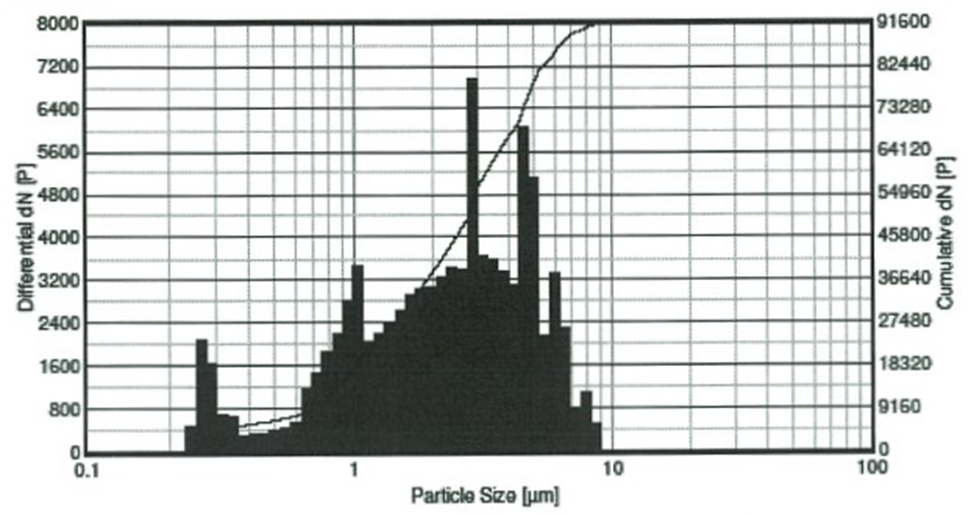
Рис. 8. Гистограмма торакального состава частиц аэрозоля на уровне головы животных в опыте. Значение модального размера частиц потока 2,868 мкм
Как следует из данных гистограммы рисунка 8, торакальный состав генерировавшегося небулайзерами аэрозольного потока в эксперименте соответствовал критериям респирабельного (размер частиц 0,5–10 мкм).
Регулировка доз аэрозоля и точность соотношения дозировок по группам достигалось посредством времяимпульсного управления работой небулайзеров. Для этого небулайзеры были дополнительно снабжены таймерами периодического включения. Период повторения включения небулайзеров составлял 4 сек. Время периодической генерации аэрозольного потока небулайзерами 4.1, 4.2, 4.3 (рис. 4) составляло: для группы 1 – 0,5 сек. (1/8 периода), группы 2 – 1,0 сек. (1/4 периода), группы 3 – 2,0 сек. (1/2 периода) соответственно. При этом суточный расход препарата составлял для групп 1 – 0,6 дм3/cут, 2 – 1,2 дм3/сут, 3 – 2,4 дм3/сут.
Фактическая средняя температура воздуха в помещении в ходе эксперимента составила значение 22 ± 2,0 °C.
Средние значения относительной влажность воздуха в лотках групп составили: 0 – 46±5,0 %, 1 – 60±3%, 2 – 82±5%, 3 – 100% + постоянное присутствие визуально наблюдаемого аэрозольного «тумана».
Определение значений объёмной концентрации серебра в воздухе лотков групп животных производилось расчётным путём.
Поступающие в воздух капли аэрозоля испаряются, вода переходит в пар, который насыщает воздух увеличивая значение его относительной влажности. Далее влажный воздух конвекционно уходит из наблюдаемого объёма, процесс повторяется и стабилизируется в устойчивом динамическом равновесии. По разности устоявшихся значений относительной влажности воздуха в лотках групп и в помещении (группа 0), учитывая значение температуры воздуха и зная содержание металла в распыляемых препаратах (20±4 мг/дм3), воспользовавшись справочными данными и соотношениями, можно выполнить расчет концентрации содержания металла серебра в воздухе которым дышали биомодели в ходе эксперимента и сопоставить полученные количественные значения с действующей нормативной базой ПДК (VOC) веществ в воздухе. Результаты расчёта приведены в таблице 7.
Таблица 7
Значения содержания металла серебро в воздухе лотков групп животных в опыте относительно значения директивных норм РФ ГН 2.2.5.3532-18 «Предельно допустимые концентрации вредных веществ в воздухе рабочей зоны»
№ группы | Отн. влажность воздуха в лотках, % | Содержание воды (пара) в воздухе при 22°С в 1 м3, мг | Содержание серебра в воздухе, мг/м3 | Содержание серебра относительно значения ПДК (1,0 мг/м3) |
0 | 46 ± 4 | 8,8 ± 0,4 (+0,0) | 0,0 | 0,0 |
1 | 63 ± 5 | 12,2± 0,5 (+3,6) | 0,072 ± 0,02 | 0,052…0,092 |
2 | 82 ± 5 | 16,1 ± 0,6 (+7,7) | 0,154 ± 0,03 | 0,124…0,184 |
3 | ˃ 100 | ˃ 19,5 (+10,7) | 0,214…0,25 | 0,214…0,250 |
Как следует из данных, приведённых в таблице 7, все группы животных в эксперименте получали дозы воздействия металла серебро содержащегося в воздухе ниже значения установленного санитарно-эпидемиологическим законодательством РФ (VOC). По факту, для основной экспериментальной группы 1 значение составило менее 0,1 ПДК, для группы 3, подвергавшейся сверхвысокой экспериментальной интенсивности воздействия технологии, не более 0,25 ПДК.
Следует отметить наличие дополнительного фактора безопасности предложенной технологии. Можно показать, что имеются принципиальные, на уровне физики процессов, ограничения, не позволяющие при использовании патопротекторов выполненных на базе ИМВК сообщать в воздух количество действующего вещества сверх установленных норм. Максимально возможное содержание металла в ИМВК связано с предельной диссоциативной способностью воды и на практике ограничено значением не более 50 мг/дм3. При введении в раствор больших количеств металл переходит из ионной в коллоидную форму и оседает на фильтрах. Для достижения концентрации металла в воздухе регламентированное нормами ПДК установленное для металла серебро 1,0 мг/м3, потребуется введение и поддержание в 1 м3 воздуха не менее 20 г раствора предельных технологически достижимых концентраций. Это возможно лишь при условии, что изначально воздух является абсолютно сухим, имеет температуру не менее 25°С и влага, поступившая из раствора, увеличивает значение относительной влажности воздуха от нулевого значения до предельно переносимого значения 90%. Реализовать передозировку активной компоненты случайным образом или намеренно на рассматриваемом технологическом уровне и условиях применения практически невозможно.
Основным ограничительным фактором для технологии следует считать ограничения, связанные с возможным переувлажнением воздуха, что подтверждают результаты эксперимента in vivo, группа 3.
7.3. Приготовление препарата ИМВК ВАХ-50
Препарат ИМВК, эквивалентный по физико-химическим и биологическим свойствам препарату ВАХ-50, в ходе эксперимента приготавливался in temporo порциями по 1,0 дм3 электролизным способом с использованием общедоступных лабораторных приборов и оборудования. Электрическая схема лабораторной установки приведена на рисунке 9.
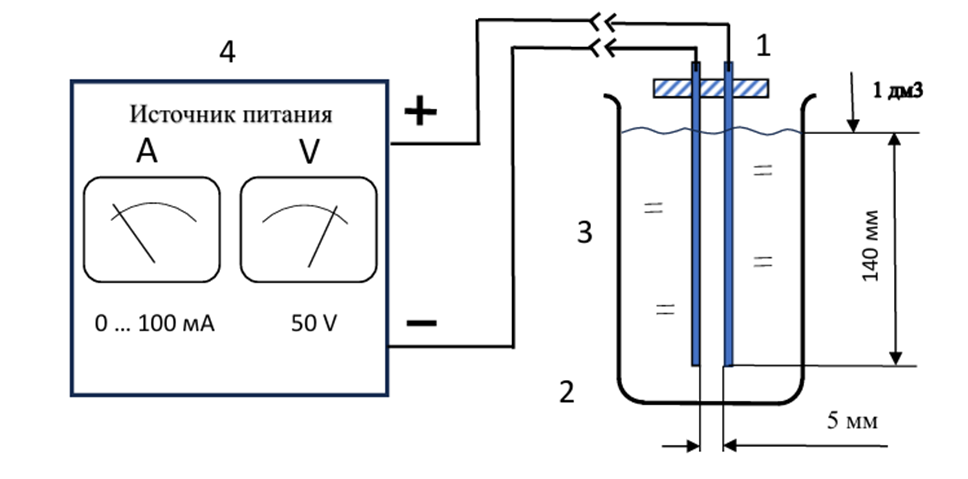
Рис. 9. Схема электрическая лабораторной установки для получения растворов ИМВК. Где: 1 – электродная группа, 2 – два серебряных электрода (стержня) диаметром 4 мм, 3 – диэлектрический прозрачный сосуд, рабочий объём 1 дм3, 4 – лабораторный источник питания с ограничением значений выходного тока 0,1 А и напряжения 50 В
Время приготовления порции препарата 1 дм3 составляет ориентировочно 35–45 минут и выполняется следующим образом:
- В сосуд 3 наливается 1 дм3 дистиллированной воды, температура 22±2,0°C.
- Устанавливается электродная группа, включается источник питания 4.
- Каждые 3–4 минуты, процесс прерывается на 0,5–1,0 минуты. Источник питания выключается, из сосуда извлекается электродная группа 1, протирочным нейтральным материалом с поверхности электродов 2 удаляются наслоения, раствор перемешивается, процесс возобновляется.
После цикла приготовления порции раствора рекомендуется изменять полярность подключения электродов к источнику питания для обеспечения равномерности их расхода.
Оперативно контролировать ход процесса растворения серебра (у других металлов эффект выражен слабо) также возможно по изменению значения силы тока в электролизной цепи. При указанной на рисунке 9 геометрии электродной группы 1, а именно, расстоянии 5 мм между электродами 2 круглой формы диаметром 4 мм и глубиной погружения электродов в раствор 140 мм, начальная сила тока электролизного процесса, при рекомендуемом значении выходного напряжении источника питания 50 V, составляет значение 2–5 мА. По мере насыщения раствора ионами серебра, электропроводимость раствора возрастает, пропорционально возрастает сила тока, проходящего через электроды. Увеличение силы тока до значения 45±3 мА при указанных условиях примерно соответствует значению удельного содержания серебра в растворе 20±4 мг/дм3.
Построение более точного калибровочного графика зависимости концентрации металла в растворе от времени обработки и силы тока в электрохимической цепи доступно для прямых гравиметрических методов. Взвешиваются электродная группа и просушенный протирочный материал. После серии циклов обработки определяется потеря массы электродной группы, вносится поправка, учитывающая изменение массы использованного, повторно просушенного, протирочного материала. Зная объём обработанной воды, определяется фактическое значение удельного содержания металла в растворе.
Хранить раствор рекомендуется в пластмассовой не электропроводящей таре в защищённом от света месте при температуре 4°C (холодильник).
Следует обратить внимание, что описанный электролизный процесс, в целом повторяя классический, имеет три отличия которые необходимо учитывать. Дистиллированная вода, особенно деионизированная, имеет очень низкие начальные показатели электропроводимости, что препятствует инициации и прохождению электролизного процесса. Общепринятый способ решения проблемы путём введения в воду различных модификаторов электрического сопротивления (соли, щелочи, кислоты), противоречит концепции ИМВК. Препятствие преодолевается путём подачи на электролизную ячейку повышенных значений рабочего напряжения. Это позволяет инициировать начальную стадию процесса, а также имеет второе значимое следствие. Существенно возрастает градиент перепада напряженности электрического поля в приэлектродном слое раствора ускоряющего и рассосредоточивающего ионы металла, которые склонны, после выхода из материала электрода, к рекомбинации в исходную металлическую форму. В рассосредоточенном состоянии ионы металла, находясь в химически чистой воде, активно образуют хорошо структурированные устойчивые гидратные оболочки, которые, фактически, выполняют в ИМВК функцию поверхностно-активных веществ обеспечивая достаточную временную стабильность растворов.
Третье отличие связано с уникальным свойством ионного серебра по мере роста концентрации кратно повышать электропроводимость водных растворов выступая тем самым в роли модификатора электрического сопротивления воды. Водный раствор, предварительно модифицированный по электропроводимости серебром, позволяет далее технологически удобным электролизным способом вводить в состав другие металлы, получать и исследовать мультиметаллические составы ИМВК.
График зависимости тока электролизной цепи (проводимости водного раствора серебра) от времени проведения процесса (роста удельной концентрации серебра в растворе) при приведенных выше условиях и геометрии электродной группы для объёма порции обрабатываемой воды 1,0 дм3 представлен на рисунке 10.
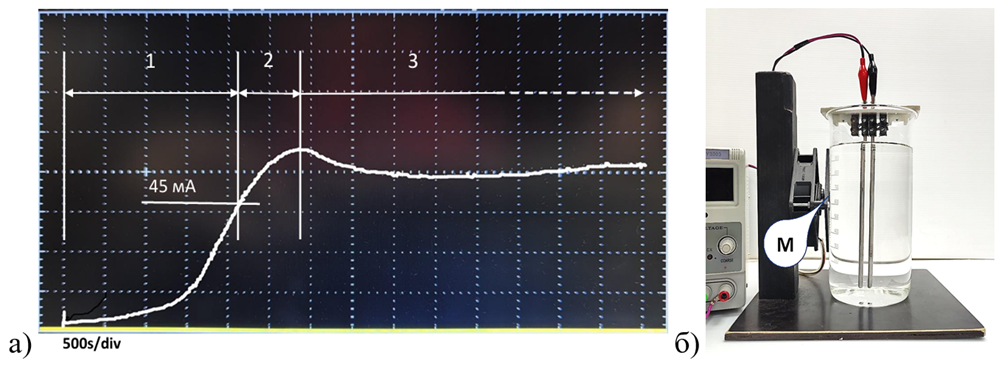
Рис. 10. График зависимости тока электролизной цепи от времени прохождения процесса а) и общий вид электролизной установки б)
Где, 1 – область инициирования процесса и формирования ионной формы серебра (целевая рабочая область процесса), 2 – переходная область, формирование фракции наноколлоидного серебра, 3 – область насыщения раствора, формирование фракции коллоидного серебра, М – магнитная мешалка вертикально–ориентированная (опция).
8. Расчётные оценки потребных количественных значений влияния патопротекторов на ход ЭП при групповом аэрозольном методе применения
Базовым элементом стратегии выживания патогенных микроорганизмов является способность к росту численности в геометрической прогрессии. Законы геометрических прогрессий симметричны, при сокращении численности патогенов действуют аналогично. Обстоятельство может быть эффективно использовано. Условием является наличие технических возможностей в периоды эпидемиологической опасности согласованно и пролонгировано воздействовать на заразное начало ЭП в местах распространения в социуме.
На практике, в соответствии с предложенной технологией (более подробно изложено в материалах описания изобретения патентного источника [1]), это означает наличие в местах возникновения или опасности возникновения ЭП парка распылительных устройств, формирующих и поддерживающих аэрозольные защитные облака патопротектора. При этом, в отличие от существующей практики проведения дезинфекционных мероприятий, предполагается возможность длительного, соизмеримого с длительностью ЭП, контакта частиц аэрозоля со всеми поверхностями защищаемого пространства включая критически важные для распространения инфекции поверхности слизистых оболочек человека и животных. То есть, при выявлении эпидемиологической угрозы, в потенциально опасных пространствах циркулирования инфекции создаются тождественные условия и пути распространения, противодействующего ей вещества – патопротектора.
При указанных условиях применения эффективность технологии на качественном уровне возможно оценить как экспериментальными методами in vivo, так и методами математического моделирования, например, воспользовавшись SIR-моделями расчета параметров ЭП [10].
Применяемая органами здравоохранения верифицированная формула расчета коэффициента распространения (коэффициента репродукции) инфекции Rt, в том числе использовавшаяся в период пандемии COVID-19 [11] выглядит следующим образом:
Rt = (Х8 + Х7 + Х6 + Х5)/ (Х1 + X2 + X3 + X4), (3)
Где X1 – X8 – число зарегистрированных больных за соответствующие сутки.
Типичными значениями Rt в РФ за 2020–2023 годы являлись: Rt = 2,0 – 4,0 для периодов вспышек заболеваемости, Rt = 0,8 – 1,6 для периодов плато и относительного затишья. Схожая ситуация наблюдалась и в других странах [12].
Допустив, что коэффициент прироста (спада) числа заразившихся за сутки монотонно одинаков в течение периода наблюдения (8 суток), из формулы (3), руководствуясь правилами геометрической прогрессии, можно определить, что суточный коэффициент изменения количества заразившихся (уровень суточной активности инфекции) составит:
![]() , (4)
, (4)
Соответственно, для значения Rt = 3,0 (среднее значение для периодов резкого роста заболеваемости), согласно (4) значение составит ![]() , при значении Rt=1,20 (типичное среднее значение для эпидемий на стадии плато) значение составит
, при значении Rt=1,20 (типичное среднее значение для эпидемий на стадии плато) значение составит ![]() . Создание препятствий на пути распространения инфекции, например механических в виде ношения масок, соблюдения социальной дистанции, самоизоляции, изоляции снижает количество поступающих в среду распространения и достигающих цели патогенов, заболеваемость снижается и наоборот, при отказе от указанных средств противодействия заболеваемость растёт. Присутствие в воздухе аэрозольных частиц патопротектора параллельно путям распространения инфекции, их осаждение с образованием защитных пленок на поверхностях слизистых, сокращающих количество патогенов способных к репродукции, имеет тот же физический смысл и последствия для динамики распространения заболевания, но с потенциально большей предсказуемостью, надежностью и эффективностью. Причины в следующем.
. Создание препятствий на пути распространения инфекции, например механических в виде ношения масок, соблюдения социальной дистанции, самоизоляции, изоляции снижает количество поступающих в среду распространения и достигающих цели патогенов, заболеваемость снижается и наоборот, при отказе от указанных средств противодействия заболеваемость растёт. Присутствие в воздухе аэрозольных частиц патопротектора параллельно путям распространения инфекции, их осаждение с образованием защитных пленок на поверхностях слизистых, сокращающих количество патогенов способных к репродукции, имеет тот же физический смысл и последствия для динамики распространения заболевания, но с потенциально большей предсказуемостью, надежностью и эффективностью. Причины в следующем.
Субъективные причины. Снижение влияния «человеческого фактора». Технология предполагает выполнение законодательно установленных норм СанПиН, VOC допустимого содержания веществ в воздухе. Это делает возможным и законным директивное применение технологии. Возможность директивного применения позволяет нивелировать возможные поведенческие издержки в исполнении противоэпидемиологических правил членами социума, обеспечивать оперативность, синхронность и общность мер противодействия при эпидемиологических угрозах.
Объективные причины. Техническая количественная малость и доступность для рассматриваемой технологии потребных уровней интенсивности воздействий, приводящих к существенным изменениям хода развития ЭП.
Критически важным первичным условием прекращения ЭП, является достижение и поддержание значения коэффициента распространения заболевания на уровне не более Rt ≤ 1,0 (соответственно Kc ≤ 1,0 согласно (4)). Относительно приведённых выше примеров это означает, что, при текущем значении Rt = 3,0 суточная активность инфекции Kc должна быть оперативно снижена в 1,32 раза, при текущем значении Rt = 1,2, в 1,047 раза соответственно. Приведённые потребные значения снижения суточной активности можно характеризовать как достаточно малые величины и, с учётом оценочных данных, полученных в ходе эксперимента in vivo, продемонстрировавшего возможность кратного снижения за короткое время (с учётом особенностей вируса – сутки) активности инфекции, возможно предположить реализуемыми для технологии.
При численном моделировании и исследовании хода ЭП с использованием как стандартных SIR так и усовершенствованных компартментных математических моделей также обращают на себя внимание и подтверждаются малые количественные уровни значений потребных влияний средств противодействия для существенных изменений хода ЭП при выполнении условий их своевременной превентивной активации, пролонгированного действия и согласованного группового применения.
9. Технологическая, экономическая и этическая составляющие метода
Насколько эффективными и успешными не были бы методы и средства противодействия инфекциям в условиях локального применения, например в рамках лечебного дела, они не имеют возможности быть действенным средством борьбы с такими природными макроявлениями как эпидемии и пандемии если не отвечают жёстким ограничивающим факторам технологической и/или экономической доступности для социума, то есть не являются возможными для массового полномасштабного применения на момент востребования.
Рамки статьи не предполагают подробное рассмотрение технико-экономической составляющей метода и технологии. Однако, следует отметить, что для промышленного производства ИМВК пригодны и достаточны существующие технологические мощности и инфраструктура по производству питьевой воды, а удельная стоимость ИМВК соизмерима либо ниже стоимости питьевой воды (в технологическом отношении питьевая вода продукт более сложный и требовательный в производстве). Также, для проверки и подтверждения тезиса о сложившейся к настоящему времени технологической и экономической доступности метода, в экспериментах in vivo автором намеренно в качестве небулайзеров применены обычные, находящиеся в широком повседневном гражданском обороте, производимые в массовых количествах, бытовые ультразвуковые увлажнители воздуха для помещений.
Для применения технологии также не просматриваются ограничения этического плана, например подобных религиозному предубеждению некоторых достаточно многочисленных групп населения к применению противоэпидемиологических веществ инвазивным и иным затрагивающим метаболизм организма способом.
10. Планы дальнейших исследований
Полученные экспериментальные и расчётные данные позволяют предположить возможность и целесообразность продолжения исследований, а именно:
- Экспериментов in vivo с совместным содержанием зараженных и не заражённых животных с целью количественных определений влияния технологии на ход ЭП в популяции, а также выполнения сопровождающих биохимических и мониторинговых рентгенологических исследований для углублённого изучения влияния технологии на защищаемые организмы.
- Расширенные исследования, включая методы молекулярного моделирования [13] и привлечение систем обработки больших баз данных, монометаллических и полиметаллических составов ИМВК с точки зрения перспективности использования в качестве веществ-патопротекторов, а также применения в аналитической химии, биохимических исследованиях, разработке новых методов и видов вакцинирующих материалов.
- С учётом выявленных практически значимых количественных результатов влияния технологии на развитие и последствия лёгочных пневмоний у биологических моделей вызванных воздействием вирусных патогенных микроорганизмов (в экспериментах наблюдалось снижение в 2,8 раза, p < 0,01, что сопоставимо с эффективностью анонсируемых к возможному появлению специализированных антивирусных препаратов), рассмотреть возможность применения патопротекторов на основе ИМВК в лечебном деле, в пульмонологии.
11. Результаты исследований и обсуждение
В работе компактно сформулирован пакет из четырёх базовых ориентирующих критериев (п. 1 – п. 4, раздел 2 статьи), который может быть полезен как для повышения продуктивности междисциплинарных взаимодействий, так и осмысления имеющихся и разработки новых направлений решения эпидемиологических задач.
Так, идея обеспечивать параллельно путям хождения инфекции тождественного ей противодействующего фактора интуитивно логична и не нова. Соответствуя п.3 и п.4 критериев, реализовывалась в средние века в виде применения противочумных костров. В работе приведён вариант научного и инженерного развития идеи до уровня, соответствующего условиям базовых критериев (п. 1 – п. 4) с учётом современных суммы знаний и возможностей технологий.
Для этого обращено внимание и использованы имеющиеся у патогенных микроорганизмов факторы уязвимости, которые ранее не рассматривались как существенно значимые либо технологически доступные внешним воздействиям:
- Геометрия. Разность размеров частиц инфекции и атакуемых ими клеток и тканей организма. Чувствительность к химическим воздействиям со стороны внешней среды на единицу объёма у малоразмерных объектов выше. В рассматриваемом контексте значительно, как правило, на порядки.
- Многими возбудителями эволюционно сформирован чрезвычайно точный и тонкий белковый механизм инвазии. Достаточно малого влияния любой, в том числе не органической, природы на структуру белков для его блокирования.
- Свойство патогенных микроорганизмов к изменению численности в геометрической прогрессии. Свойство повышает вероятность выживания инфекции при разовых мощных нейтрализующих воздействиях, но обуславливает повышенную чувствительность к умеренным воздействиям длительных экспозиций.
- Узость ворот входа-выхода воздушно-капельных инфекций. Наличие на границе раздела сред естественного наноразмерного по толщине «игольного ушка» в виде поверхности слизистых.
В ходе выполнения работ предложен проект технического решения, реализующего метод [1]. Проверены ключевые аппаратные компоненты технологии в опытах in vivo.
Введены понятия и рассмотрены поддерживающие технологию группы специализированных веществ – ИМВК и веществ – патопротекторов на их основе.
Показана возможность изучения процессов распространения ЭП и влияния на него предложенной аэрозольной технологии с использованием в качестве модельной среды распространения инфекции лёгочных тканей животных.
Приведены необходимые для воспроизведения сведения и подробности о технических средствах поддержки технологии.
Представлены результаты поддерживающих пошаговых оценочных исследований предложенного метода in vitro и in vivo.
В целом, полученные результаты работ позволяют предположить, что предлагаемые метод и технология могут рассматриваться как интеллектуально, технологически, организационно и экономически доступные, не противоречащие, совместимые и дополняющие по отношению к существующим методам и средствам противодействия распространению инфекций. Учитывая сформировавшийся социальный заказ на разработку дополнительных, качественно новых методов и средств противодействия эпидемиологическим угрозам, целесообразно дальнейшее изучение и развитие направления.
Конфликт интересов:
Работа выполнялась в инициативном порядке. Внешнего финансирования и иных форм поддержки проекта не имелось. Автор заявляет об отсутствии конфликтов интересов.
Благодарности:
Автор выражает особую признательность за уделённое внимание, обсуждение, критические замечания и рекомендации по работе академику РАН, д.м.н., проф. А. Г Чучалину, заслуженному деятелю науки РФ, д.м.н., профессору В. Т. Долгих, а также; д.б.н., Л. А. Краевой, д.б.н. В. В. Зарубаеву, к.м.н. В. А. Гомболевскому, к.м.н. К. В. Кокорину, инженерам Л. В. Лементуеву и А. Г. Худякову.
Благодарит за участие и поддержку в работах по подготовке и проведению экспериментов сотрудников:
- Лаборатории экспериментальной вирусологии, лаборатории медицинской бактериологии. ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека».
- Лаборатории токсикологии ИЦГО, лаборатории токсикологической химии неорганических соединений. ФГБУ НКЦТ им. С. Н. Голикова ФМБА России.
- Центра экспериментальной фармакологии. Санкт-Петербургский государственный химико-фармацевтический университет.
- Испытательной химико-аналитической лаборатории. АО «ГосНИИхиманалит», г. Санкт-Петербург, Россия.
- Компании ООО «Нью-Лайн», г. Санкт-Петербург, Россия.
.png&w=384&q=75)
.png&w=640&q=75)