В современном мире, учитывая развитие инновационных технологий, изыскание новых биологически активных соединений, применяемых в качестве лекарственных препаратов, всё ещё остается одной из основных задач органической химии и фармакологии. Решение данной задачи ведётся, как по линии выявления активных биологических соединений среди продуктов химического синтеза и природных веществ, так и по линии целенаправленного синтеза.
По данным автором [1], производные 2-амино-1,3,4-тиадиазола обладает широкого спектра противораковых активности, которые были получены из соответствующих альдегидов или карбоновых кислот. Oни оказался хорошим кирпичам для построение конденсированных имидазо[2,1-b][1,3,4]-тиадиазольных циклов, что некоторые этих соединений обладают противораковый [2], противотуберкулезный [3], антибактериальный [4] и противогрибковый [5] свойств. Кроме того, некоторые соединения, содержащие имидазо[2,1-b][1,3,4]-тиадиазольной фрагмент используется как противовоспалительное [6], кардиотоническое [7], мочегонное [8] и гербицидное [9] агенты и используются для производства красителей [10].
В связи с этим настоящая статья сосредоточились на синтезе новых конденсированных имидазо[2,1-b][1,3,4]-тиадиазолов - 2-бром- и 2-фенил-6-(пара-метилфенил)-имидазо[2,1-b][1,3,4]-тиадиазолы 4-5. В качестве исходных материалов для синтеза соединений 3-4 была выбрана 2-амино-5-бром/фенил-1,3,4-тиадиазолы 1-2 и 2-бром-1-п-толилэтанона 3. В среде бутанол-1 при нагревание соединение 1-2 с 2 в течение 5-6 ч. они были превращены в 4-5 с хорошими выходами.
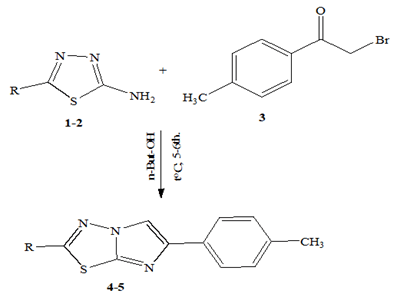
R = Br (1, 3); Ph (2, 5)
Контроль за ходом реакции и чистота полученного соединения осуществляли методом ТСХ на пластинке «Silufol UV-254» с проявлением паров йода. Строения 4-5 подтверждено ИК-спектральными данными. ИК-спектры полученных соединений была записана в виде кристаллическом образце на спектрометр Spectrum 65 FT-IR (Perkin Elmer) который оснащен MIRACLE ATR (ZnSe) в Институте химии им. В.И Никитина НАНТ. Каждый записанный спектр был получен в среднем на 16 - 20 сканирований, которые варьировались от 4000 - 600 см-1 с разрешением 4 см-1. Перед измерении образцы были высушены для фонового спектра. Записанные каждые спектры были проанализирован и установлен с помощью программного обеспечения Perkin Elmer Spectrum, версии 10.03.071.
В ИК-спектре соединений 4-5 в кристаллическом состояние, имеются интенсивной полосы поглощении характерно для имидазо[2,1-b][1,3,4]-тиадиазольного кольцо и экзоциклический функциональных групп.
В спектре 3 присутствуют полосы поглощения в области 1541, 1491, 1456 и 679 см-1 характерные для C=N, C=C и C-S-C-тиадиазоло-имидазольного фрагменты, а для экзоциклический функциональных групп имеется полосы поглощении валентной колебании для C-Br и пара-СН3-C6H4-группы присутствуют в области 565 и 3048 см-1.
В спектре 4 обнаружено полоса поглощении при 1632, 1530, 1488 и 680 см-1 характерно для C=N, C=C и C-S-C-тиадиазоло-имидазольного фрагменты. Для фенильной группы 2-го положения гетероцикла полоса поглощения обнаружено в области 3072 см-1, а для пара-метилфенильного группа полоса поглощении проявлено в области «отпечаток палец» при 1019-1056 см-1.
Таким образом, наличие заместителей 2 и 6 положение данного гетероцикла, влияют на распределение электронной плотности, что происходит изменении в интенсивности некоторых пиков данного соединения. В ИК-спектре соединения 4-5, обнаружены характерные полосы поглощения имидазо-тиадиазольного цикла, экзоциклический функциональных групп 2 и 6 положении и других полосы относящиеся данных гетероциклов, что соответствуют литературным данным [10-11].
Авторы выражают глубокую благодарность д.х.н., профессору Мухидинову З.К. и его рабочей группе за оказание помощи при выполнении спектральных исследований.

.png&w=640&q=75)