Фитопланктон играет ключевую роль в биогеохимических циклах и широко используется в фундаментальных и прикладных исследованиях – от мониторинга состояния водных экосистем до получения биомассы для биотехнологических и фармацевтических целей [1, с. 544-555]. Однако одной из основных проблем является эффективное выделение фитопланктона из природной или модельной водной среды. Традиционные методы, включая фильтрацию, центрифугирование и флотацию, часто ограничены низкой производительностью, разрушением клеток или высокими энергетическими затратами [2, с. 22-26]. В связи с этим актуальной задачей является разработка и оптимизация методов интенсификации процесса выделения фитопланктона.
На сегодняшний день применяются следующие основные методы: механические (фильтрация, мембранные технологии, центрифугирование) [2, с. 22-26], физико-химические (флотация, коагуляция, электрофорез), инновационные технологии (магнитная сепарация с использованием функционализированных наночастиц, микрофлюидные устройства) [3].
Каждый метод обладает специфическими преимуществами и ограничениями, что обусловливает необходимость комплексного анализа и поиска оптимальных решений для различных условий.
Целью работы является оценка эффективности метода пробного коагулирования для интенсификации процесса выделения фитопланктона из воды и определение оптимальных условий применения данного метода.
Реагентные методы очистки вод от фитопланктона представляют собой эффективные технологии, направленные на снижение концентрации микроскопических водорослей в водоемах и сточных водах. Эти методы основываются на использовании химических реагентов, которые способствуют коагуляции и флокуляции клеток фитопланктона, облегчая их последующее отделение из воды. Одним из наиболее распространенных реагентов является хлорид алюминия, который действует как коагулянт [4]. Он способствует образованию более крупных агрегатов клеток водорослей, что значительно увеличивает их осаждение. При этом важно правильно подбирать дозировку реагента, так как избыточное количество может негативно сказаться на экосистеме водоема.
Другим широко используемым в данных целях реагентом является оксид алюминия в форме сульфата алюминия. Он является эффективным коагулянтом для очистки вод от фитопланктона [5, с. 48-59]. При добавлении в воду он способствует образованию крупных агрегатов клеток водорослей, что облегчает их осаждение. Процесс коагуляции происходит за счет нейтрализации электрических зарядов на поверхности клеток, что приводит к их сцеплению [5, с. 48-59]. Оксид алюминия также может улучшать качество воды, снижая мутность и концентрацию питательных веществ.
Важно отметить, что реагентные методы требуют тщательного контроля за качеством воды и возможными побочными эффектами. Применение химических реагентов может привести к изменению химического состава воды и повлиять на другие организмы в экосистеме. Поэтому перед использованием этих методов необходимо проводить предварительные исследования и тестирования.
Для оценки воздействия реагентов при очистке воды от фитопланктона был проведен эксперимент, основанный на методе «пробного коагулирования».
В качестве фитопланктона был выбран морской фитопланктон «Gold» Isochrysis galbana (рис. 1).

Рис. 1. Используемый в эксперименте фитопланктон «Gold»
В качестве первого реагента был выбран раствор сульфата алюминия, массовая доля основного вещества Al2O3=7,5%, производитель ООО «НПО «Завод химических реагентов»» (рис. 2) [6].
Характеристики реагента представлены в таблице 1 [6].
Таблица 1
Характеристики водного раствора сульфата алюминия
Наименование показателя | Норма |
Массовая доля оксида алюминия, %, не менее | 6,8–7,7 |
Массовая доля нерастворимого в воде остатка, %, не более | 0,3 |
Массовая доля железа в пересчете на оксид железа (III), %, не более | 0,02 |
Массовая доля свободной серной кислоты, (H2SO4), %, не более | 0,15 |
Массовая доля мышьяка в пересчете на оксид мышьяка (III), %, не более | 0,0015 |
Цвет | Жидкость с желтоватым или серым оттенком |

Рис. 2. Флакон с реагентом водный раствор сульфата алюминия
В два мерных цилиндра были добавлены по 50 мл фитопланктона. Доза реагента в первом случае – 1 мл, во втором – 2 мл. В течение 30 минут данные концентрации реагента не дали результата, из чего был сделан вывод, что применение сульфата алюминия неэффективно в случае очистки воды от используемого в опыте фитопланктона. Результаты эксперимента по истечении 30 минут представлены на рисунке 3.

Рис. 3. Результаты эксперимента с использованием водного раствора сульфата алюминия
Далее в исследовании был использован другой реагент – композиционный реагент ОПТИОКС‑П производства ООО «НПО «Завод химических реагентов»». Данный реагент представляет собой многокомпонентную композицию на основе соединений алюминия, предназначенную для процессов коагуляции и флокуляции в системах водоподготовки и очистки сточных вод [6].
Ключевой активный компонент реагента – оксид алюминия (Al2O3), массовая доля которого составляет 23,4%. Высокое содержание Al2O3 обеспечивает эффективную нейтрализацию заряда взвешенных частиц и коллоидных систем, что способствует их быстрому слипанию (коагуляции) и последующему осаждению.
Технические характеристики и данные о производителе подтверждены сопроводительной документацией и представлены на рисунке 4 [6].

Рис. 4. Флакон с реагентом ОПТИОКС-П
Композиционный реагент ОПТИОКС-П представляет собой современный коагулянт, применяемый для очистки природных, хозяйственно-питьевых и сточных вод различного происхождения. Он является аналогом гидроксохлорида алюминия и относится к группе алюмосодержащих коагулянтов с повышенной флокулирующей способностью. Механизм его действия основан на дестабилизации коллоидных и взвешенных частиц с последующим образованием крупных агрегатов (хлопьев), что существенно ускоряет их осаждение и повышает эффективность процессов водоочистки [7]. Благодаря более высокой концентрации активного вещества (в пересчете на Al₂O₃) и оптимизированному химическому составу, такие реагенты обеспечивают более интенсивное хлопьеобразование по сравнению с традиционными коагулянтами, что делает их перспективными для интенсификации процессов удаления микроводорослей и других дисперсных загрязнений из воды [6].
Характеристики реагента представлены в таблице 2 [6].
Таблица 2
Характеристики композиционного реагента ОПТИОКС-П
Наименование показателя | Норма |
Массовая доля основного вещества в пересчете на оксид алюминия (Al₂O₃), %, в пределах | 10–26 |
Массовая доля хлоридов, %, в пределах | 3,5–21 |
Атомное отношение алюминия к хлору АМ/СІ, в пределах | 0,5–0,22 |
Массовая доля железа в пересчете на оксид железа (Fe₂O₃), %, не более | 0,2 |
Водородный показатель, ед. рН | 1,0–5,0 |
Плотность, кг/дм3 | 1,08–1,5 |
Массовая доля полиДАДМАХ, %, не более | 2,0 |
Массовая доля остаточного мономера (ДАДМАХ), %, не более | 0,02 |
Цвет | Раствор светло-желтого либо серого цвета с зеленоватым оттенком, допускается наличие мути |
Для первого эксперимента с данным реагентом были использованы дозы в 3 и 5 мл на тот же объем фитопланктона – 50 мл. В результате через 30 минут в цилиндре с 3 мл образовались хлопья (рис. 5), которые были рассмотрены более детально под микроскопом (рис. 6). В случае с 5 мл никакой реакции не произошло, из чего был сделан вывод, что такая концентрация вещества – избыточна при решении задачи очистки воды от фитопланктона.

Рис. 5. Результаты применения реагента ОПТИОКС-П (слева – направо контроль, 3 мл, 5 мл)
На рисунке 6 представлены фото сформировавшихся в результате коагуляции агрегатов клеток фитопланктона. Наблюдается объединение отдельных клеток в более крупные хлопьевидные структуры, что подтверждает эффективность процесса коагуляции при использовании исследуемого реагента ОПТИОКС-П.
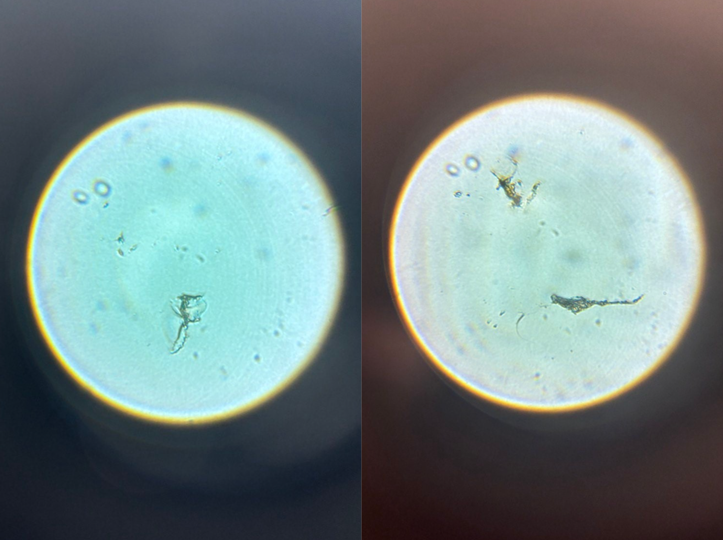
Рис. 6. Хлопья фитопланктона под микроскопом
С целью определения оптимальной дозы реагента для эффективного осаждения фитопланктона был проведён повторный эксперимент. В ходе исследования тестировались следующие дозировки реагента: 1 мл, 2 мл, 2,5 мл, 3,5 мл и 4 мл. Каждая дозировка вводилась в отдельный цилиндр с идентичной исходной суспензией фитопланктона для обеспечения сопоставимости результатов.
Наблюдение за процессом флокуляции (образования хлопьев) проводилось в течение фиксированного периода времени. Спустя 30 минут после внесения реагента визуально было зафиксировано начало формирования хлопьев фитопланктона в цилиндрах, содержащих дозы 2,5 мл и 3,5 мл (рис. 7). Это указывало на достижение пороговой концентрации реагента, достаточной для запуска процесса коагуляции.

Рис. 7. Результаты эксперимента после 30 минут при дозах 2,5 мл и 3,5 мл
В ёмкостях с остальными протестированными концентрациями (1 мл и 2 мл, а также 4 мл) в течение наблюдаемого периода не произошло каких‑либо визуально фиксируемых изменений в состоянии суспензии (рис. 8). Отсутствие хлопьеобразования при низких дозах (1 мл и 2 мл) свидетельствует о недостаточной концентрации реагента для преодоления сил электростатического отталкивания между клетками фитопланктона. Отсутствие улучшений при дозе 4 мл может указывать на достижение насыщения или на отсутствие дополнительного эффекта от дальнейшего увеличения дозы в данных условиях.

Рис. 8. Результаты эксперимента после 30 минут при дозах 4 мл, 2 мл и 1 мл
Для достоверности проведённого эксперимента было принято решение оценить результаты спустя сутки после добавления реагента. Это позволило проследить динамику осаждения хлопьев фитопланктона и оценить стабильность процесса в долгосрочной перспективе.
В итоге наиболее удачный вариант был получен при добавлении 4 мл реагента на 50 мл раствора фитопланктона. В этом случае образовался плотный осадок, а вода достигла максимального уровня осветления – что наглядно продемонстрировано на рисунке 9.

Рис. 9. Результат эксперимента спустя сутки с дозой реагента 4 мл
Проведённые исследования показали принципиальные различия в эффективности традиционного и композиционного коагулянтов при очистке воды от золотистого фитопланктона. Установлено, что использование водного раствора сульфата алюминия в применённых дозировках не приводит к образованию хлопьев и, следовательно, не обеспечивает осветления среды. В то же время применение композиционного реагента ОПТИОКС-П продемонстрировало выраженный коагуляционный эффект.
Экспериментально определено, что оптимальная доза ОПТИОКС-П составляет 4 мл на 50 мл исходного раствора фитопланктона, что соответствует концентрации порядка 7,4%. При данной дозировке наблюдается максимальное осветление воды и образование устойчивого осадка, что позволяет рассматривать данный реагент как более перспективное средство по сравнению с традиционным сульфатом алюминия.
Полученные результаты представляют интерес не только для лабораторных исследований и задач концентрирования биомассы фитопланктона, но и для разработки технологических схем очистки природных и сточных вод. Перспективными направлениями дальнейших исследований являются уточнение влияния внешних факторов (pH, температура, состав водной среды) на процесс коагуляции, определение диапазона эффективных дозировок реагента для различных видов фитопланктона, а также апробация методики в проточных системах, приближённых к реальным условиям эксплуатации.
Таким образом, применение коагулянтов может рассматриваться как эффективный и технологически оправданный способ интенсификации процессов очистки воды от фитопланктона.
.png&w=384&q=75)
