В районах добычи нефти содержание ряда элементов часто повышается в связи с тем, что они извлекаются на поверхность вместе с нефтью или производственной деятельностью при добыче нефти. Промышленные предприятия, увеличиваясь с каждым годом, производят все большее количество сбросов и выбросов, загрязняющих окружающую среду. Среди этих загрязнителей самыми устойчивыми являются тяжелые металлы [4]. Известно, что в определенных концентрациях они не только влияют на качество пресных вод, но и становятся токсичными для гидробионтов и аккумулируются в их тканях. По трофическим цепям металлы могут попадать в организм человека [2]. Не менее значимой экологической проблемой для пресных водоемов является засоление, в частности увеличение содержания хлоридов и сульфатов. Увеличение содержания тяжелых металлов и повышение солености в пресноводных экосистемах приводят к угнетению ростовых характеристик фитопланктона [4].
Целью данной работы является оценка влияния ионов меди на рост численности клеток тест-культуры Chlorella vulgaris при повышенном содержании хлорида натрия в среде.
Для определения путем биотестирования токсичности солей тяжелых металлов на живые организмы, тест-объектом выбрана одноклеточная водоросль Chlorella vulgaris, так как у них короткий жизненный цикл, что позволяет наблюдать изменения [5].
Методика основана на измерении различий в оптической плотности водорослей Chlorella vulgaris, выращенных в нетоксичной среде (контроль), и испытуемых образцов, содержащих токсичные вещества [1].
В ходе проведения эксперимента оценивали влияние токсикантов (CuCl2; NaCl), а также их комбинированное действие на рост и одноклеточной зеленой водоросли Chlorella vulgaris. Результаты влияния NaCl в концентрациях (мг/л): 2000; 1500; 1000; 500; 300 на численность клеток водоросли представлены на рисунке 1.
Для оценки токсичности тяжелых металлов использовали соль CuCl2 с концентрациями: 0,0001, 0,001, 0,01, 0,1 и 1 мг/л. Для моделирования засоления водной среды использовали NaCl с концентрациями 2000; 1500; 1000; 500; 300 мг/л.
Для определения токсического действия при комбинированном воздействии тяжелых металлов и засоления приготовили раствор хлорида меди в концентрациях 0,00001, 0,0001, 0,001, 0,01, 0,1 мг/л и хлорида натрия в концентрациях 300 и 700 мг/л. Каждую концентрацию растворов делали в четырёхкратной повторности. Растворы готовили на дистиллированной воде. Токсичной для водоросли принималось снижение оптической плотности суспензии на 20 процентов и более.
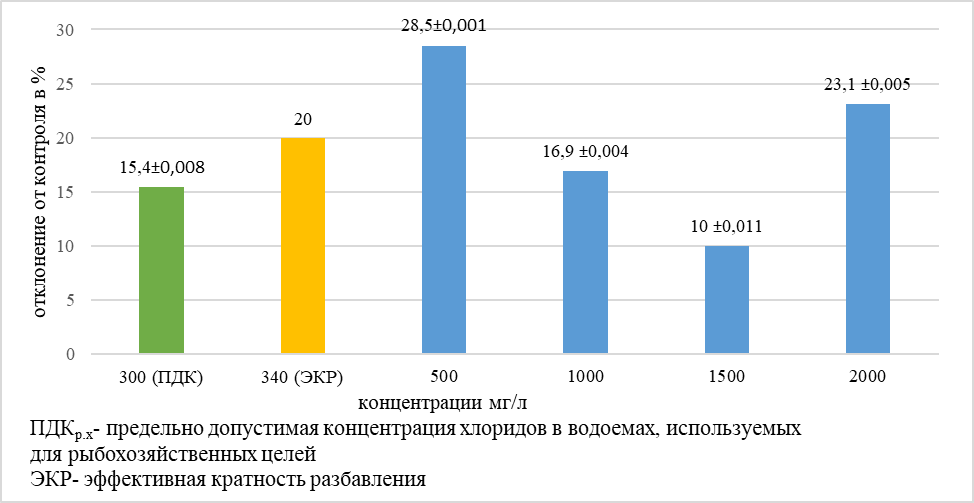
Рис. 1. Относительная разница между величинами тест-реакции для каждого разведения по сравнению с контролем (в %)
Из представленных данных видно, что при концентрации, соответствующей ПДКр.х для хлоридов (300 мг/л) отсутствует токсический эффект, тестируемая проба не оказывает острого токсического действия. В концентрациях 500 и 2000 мг/л мы наблюдаем токсический эффект (угнетение роста на 28,5 и 23,1 процента соответственно). При концентрации токсиканта 340 мг/л происходит подавление роста культуры микроводоросли Chlorella vulgaris на 20 процентов по сравнению с контролем.
Ссылаясь на результаты, представленные в работе Н. О. Жила, Г. С. Калачевой и Т. Г. Воловой, можно предположить, что микроводоросли демонстрируют повышенную жизнеспособность в условиях слабосолоноватой среды (с концентрацией солей 1000–2000 мг/л) по сравнению с условиями нормальной пресной воды (500–1000 мг/л) [3, с. 229-242].
Выявленная устойчивость пресноводных зеленых микроводорослей к увеличению концентрации солей может свидетельствовать об их потенциальной галофильности. Среди зеленых микроводорослей, такие как Chlorella, Scenedesmus и Chlorococcum, продемонстрировали способность к пролиферации в условиях повышенной солености. Механизмы такой адаптации, вероятно, включают осмотическую регуляцию, обеспечивающую сохранение внутриклеточного потенциала воды, и защиту клеточных белков от денатурации, что способствует выживаемости организмов в условиях с высокой соленостью.
Ч. З. Тимергалиева в своей работе показала, что при концентрации 0,01 мг/л хлорид меди начинал проявлять своё элиминирующее воздействие на водоросли. При этом даже малые дозы хлорида меди (0,001 мг/л) могли вызывать первые признаки плазмолиза клеток, что приводило к изменению их формы с шаровидной на эллиптическую форму, в то время как в нормальном состоянии клетки хлореллы имеют шаровидную форму [6, с. 23-29].
На рисунке 2 представлены результаты расчета оптической плотности суспензии микроводоросли при действии хлорида меди.
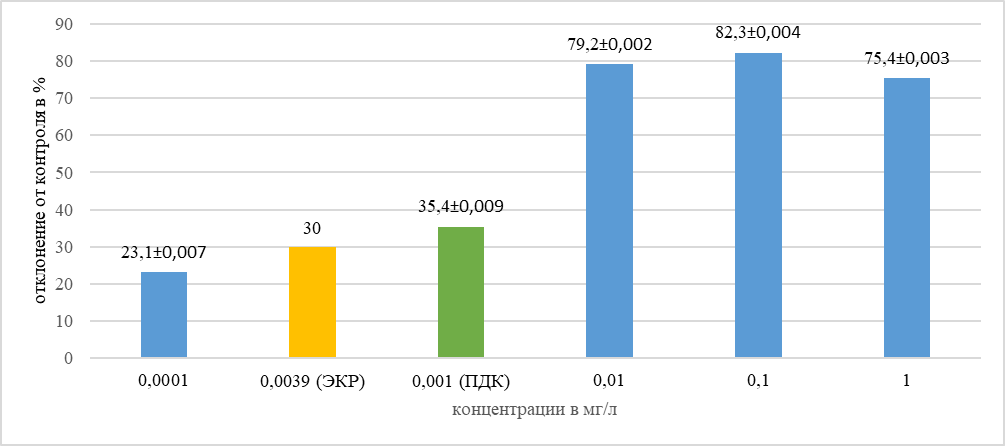
Рис. 2. Относительная разница между величинами тест-реакции для каждого разведения по сравнению с контролем (в %)
Эксперимент с использованием хлорида меди показал, что с увеличением концентрации ионов меди в растворе оптическая плотность суспензии водоросли снижается. Снижение оптической плотности на 23 процента наблюдается в концентрации 0,0001 мг/л. Снижение оптической плотности на 30 процентов происходит в растворе хлорида меди с концентрацией 0,0039 мг/л.
При концентрации, соответствующей ПДКр.х по меди (0,001 мг/л) зафиксирован токсический эффект, отклонение оптической плотности от контроля составило 35,4 процента.
Результаты влияния CuCl2 и NaCl 300 мг/л на численность клеток водоросли представлены на рисунке 3.
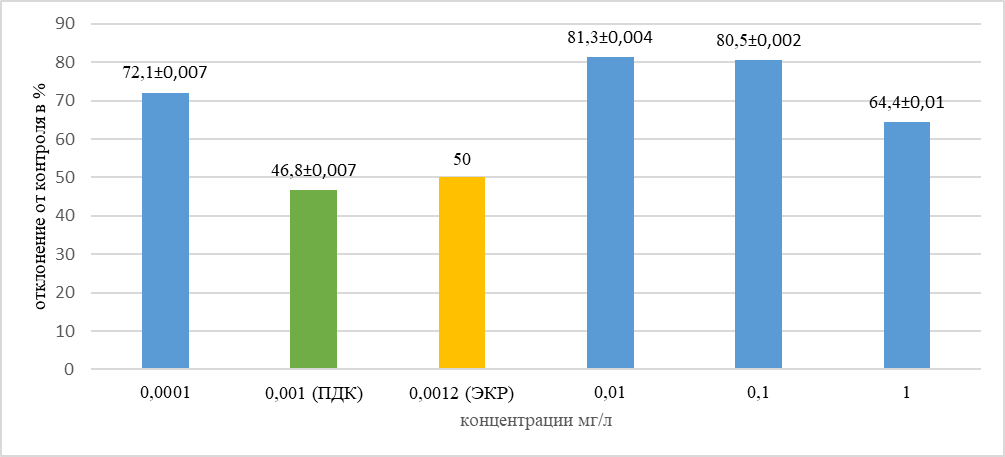
Рис. 3. Относительная разница между величинами тест-реакции для каждого разведения по сравнению с контролем (в %)
При концентрации, соответствующей ПДКр.х по меди (0,001 мг/л) был зафиксирован токсический эффект, отклонение от контроля составило 46,85 процента. В остальных концентрациях отклонение от контроля составило 64 и более процентов. По полученным данным рассчитали ЭКР50, который равен 0,0012 мг/л.
Результаты комбинированного влияния CuCl2 и NaCl 700 мг/л на численность клеток водоросли представлены на рисунке 4.
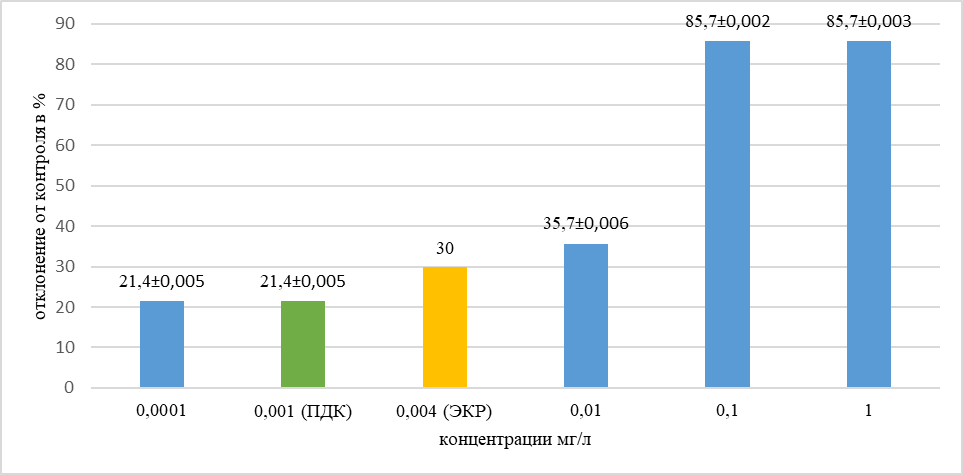
Рис. 4. Относительная разница между величинами тест-реакции для каждого разведения по сравнению с контролем (в %)
Эксперимент с комбинированным действием солей меди и хлорида натрия в концентрации 700 мг/л показал, что при увеличении концентрации ионов меди увеличивается ингибирующий эффект.
При концентрации, соответствующей ПДК для рыбохозяйственных водоемов по меди (0,001мг/л) был зафиксирован токсический эффект, отклонение от контроля составило 21,4 процента.
Наибольшее отклонение от контроля обнаружено в концентрациях 0,1 и 1 мг/л и составило 85,7 процента. Снижение оптической плотности на 30 процентов происходит в варианте опыта с концентрацией хлорида меди концентрации 0,004 мг/л.
В результате выполненных исследований установлено, что тест-культура микроводоросли Chlorella vulgaris способна адаптироваться к хлоридному засолению. Концентрации хлорида натрия в диапазоне от 300 мг/л до 2000 мг/л незначительно снижают рост численности клеток.
При изолированном действии хлорид меди снижается рост численности клеток водоросли Chlorella vulgaris в концентрациях выше ПДК р.х. В концентрациях ниже ПДК р.х токсическое действие металла на рост численности клеток тест-культуры не выявлено.
Комбинированное действие тяжелых металлов на уровне ПДК р.х и хлорида натрия в концентрациях 300 и 700 мг/л оказывает больший токсический эффект чем при изолированном воздействии тяжелых металлов на тест-культуру Chlorella vulgaris, что проявляется в угнетении роста численности клеток микроводоросли.
.png&w=384&q=75)
