Актуальность исследования
Нарушения сердечного ритма являются одними из наиболее частых и клинически значимых осложнений в послеоперационном периоде у пациентов, перенёсших хирургические вмешательства на сердце. По данным различных исследований, фибрилляция предсердий, желудочковые тахиаритмии и брадикардии возникают у 15–60% пациентов после кардиохирургических операций, увеличивая риск инсульта, сердечной недостаточности, продлевая срок госпитализации и повышая стоимость лечения.
Современные достижения в кардиохирургии и анестезиологии позволяют улучшать исходы операций, однако послеоперационные аритмии остаются значимым фактором, влияющим на прогноз и качество жизни пациентов. В связи с этим особую значимость приобретает разработка эффективных стратегий профилактики и методов коррекции нарушений ритма, адаптированных к конкретным клиническим ситуациям.
Необходимость комплексного подхода к ведению таких пациентов с учётом индивидуальных рисков, современного арсенала медикаментозной и интервенционной терапии делает тему исследования актуальной для кардиологической и реаниматологической практики.
Цель исследования
Целью данного исследования является анализ современных подходов к профилактике и лечению нарушений сердечного ритма у пациентов после хирургических вмешательств на сердце, с акцентом на выбор оптимальных тактик ведения в зависимости от клинической ситуации, характера операции и индивидуальных факторов риска.
Материалы и методы исследования
Использованы данные из международных клинических рекомендаций, публикации в рецензируемых медицинских журналах и результаты многоцентровых клинических исследований.
Методологической основой послужил систематический анализ литературы. Были обобщены сведения по классификации аритмий, методам профилактики, показаниям к терапии, тактике лечения и долгосрочному прогнозу. Проведен сравнительный анализ эффективности различных антиаритмических стратегий по данным метаанализов и когортных исследований.
Результаты исследования
Развитие нарушений сердечного ритма в послеоперационный период является следствием множества взаимосвязанных патофизиологических процессов, развивающихся на фоне хирургической травмы миокарда, воспалительной реакции и электролитного дисбаланса. Эти аритмии представляют собой результат комплексного воздействия как интраоперационных факторов, так и изменений, происходящих в раннем послеоперационном периоде.
К числу основных этиологических факторов относят:
- Механическое повреждение проводящей системы сердца, особенно при операциях, включающих коррекцию клапанных пороков или вмешательства на перегородках, где риск травмы атриовентрикулярного (AV) узла и пучков Гиса повышен [5, с. 62].
- Ишемия миокарда, возникающая в результате временного пережатия коронарных сосудов или в условиях неполной реперфузии после снятия аортального зажима.
- Воспалительная реакция, запускаемая искусственным кровообращением (ИК), с выбросом цитокинов, активацией лейкоцитов и повреждением мембран кардиомиоцитов.
- Нарушения электролитного обмена, особенно гипокалиемия, гипомагниемия и гипокальциемия, которые критически влияют на стабильность клеточного потенциала и проведение импульсов.
- Изменения вегетативной регуляции, преимущественно повышенный тонус симпатической нервной системы, способствующий развитию фибрилляции предсердий и других тахиаритмий [3, с. 9].
Патогенез послеоперационных аритмий включает ряд ключевых механизмов:
- Электрофизиологическая нестабильность, обусловленная постишемической деполяризацией клеточных мембран, снижением проводимости и повышением автоматизма в эктопических очагах.
- Дисфункция и ремоделирование предсердий, особенно в условиях дилатации и фиброза, приводит к формированию субстрата для повторного входа возбуждения, что особенно характерно для фибрилляции предсердий [2, с. 33].
- Повышение уровня провоспалительных медиаторов (интерлейкины 6 и 8, С-реактивный белок), связанных с кардиохирургической операцией, оказывает влияние на ионные каналы, модулируя проводимость миокарда.
- Раздражение перикарда и околосердечных структур вследствие хирургических манипуляций также способствует запуску аритмогенных очагов.
Частота встречаемости послеоперационных аритмий описана в таблице 1.
Таблица 1
Частота встречаемости послеоперационных аритмий
№ | Тип аритмии | Частота встречаемости (% пациентов) | Примечание |
1 | Фибрилляция предсердий (ФП) | 25–40% | Наиболее частая аритмия после АКШ и клапанных операций |
2 | Желудочковые тахиаритмии | 8–15% | Часто связаны с ишемией и рубцовыми изменениями |
3 | Синусовая брадикардия | 5–10% | Может требовать временной ЭКС (электрокардиостимуляции) |
4 | Атриовентрикулярная блокада (AV-блок) | 3–7% | Особенно при вмешательствах на клапанах и перегородке |
5 | Суправентрикулярная тахикардия (СВТ) | 2–5% | Часто проходит самостоятельно, требует наблюдения |
6 | Фибрилляция желудочков (ФЖ) | <1% | Жизнеугрожающее состояние, требует немедленной дефибрилляции |
Послеоперационные аритмии классифицируются на основе электрофизиологических механизмов возникновения, что позволяет формировать патогенетически обоснованные подходы к их диагностике и лечению. Аритмии подразделяются на четыре основных класса (табл. 2).
Таблица 2
Классификация и клинические проявления послеоперационных аритмий
№ | Класс аритмии | Типичные формы |
1 | Нарушения автоматизма | Синусовая тахикардия, синусовая брадикардия |
2 | Нарушения проводимости | Атриовентрикулярная блокада (I–III ст.), блокада ножек пучка Гиса |
3 | Аритмии re-entry (ре-энтри) | Фибрилляция предсердий, трепетание предсердий |
4 | Триггерные аритмии | Желудочковая тахикардия, суправентрикулярная тахикардия с акцессорными путями |
Такая классификация имеет клиническое значение, так как позволяет целенаправленно выбирать стратегию коррекции в зависимости от механизма аритмии.
Ниже приведена диаграмма, отражающая частоту госпитализаций по основным типам послеоперационных аритмий (рис. 1).
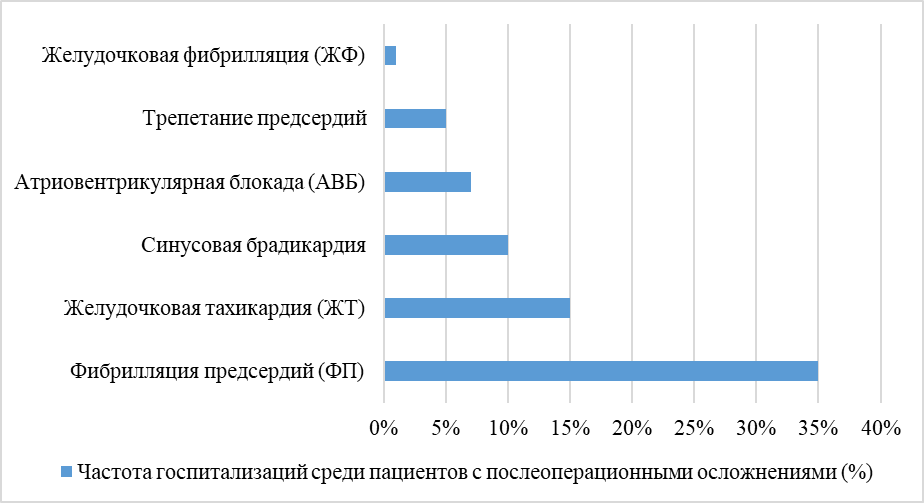
Рис. 1. Частота госпитализаций из-за послеоперационных аритмий
Из представленных данных видно, что фибрилляция предсердий остаётся ведущей причиной послеоперационной аритмогенной нестабильности, за ней следуют желудочковые аритмии и различные формы блокад. Эти состояния требуют своевременной диагностики и дифференцированного подхода к лечению [1, с. 15].
Профилактика послеоперационных аритмий является важным направлением в кардиохирургической практике, так как позволяет снизить частоту осложнений, продолжительность госпитализации и потребность в интенсивной терапии. Современные стратегии профилактики основаны на патогенетических механизмах аритмогенеза и включают медикаментозные, коррекционные и организационно-хирургические подходы.
Амиодарон, применяемый в режиме пероральной или внутривенной загрузки до и после операции, демонстрирует наивысшую эффективность в профилактике фибрилляции предсердий. Применение амиодарона снижает риск послеоперационной ФП более чем на 50% у пациентов с повышенным риском.
Бета-блокаторы, особенно бисопролол и метопролол, остаются базисной терапией, показавшей снижение риска развития аритмий на 30%, за счёт уменьшения симпатической активности и стабилизации проводящей системы сердца. Их использование рекомендуется начинать за несколько дней до операции и продолжать в раннем послеоперационном периоде.
Антагонисты кальция, преимущественно недигидропиридиновые (верапамил, дилтиазем), эффективны в снижении частоты наджелудочковых тахиаритмий, особенно у пациентов с непереносимостью бета-блокаторов. Они показали эффективность порядка 20% при профилактике СВТ.
Коррекция электролитных нарушений, в частности уровней калия и магния, играет важную роль в стабилизации мембранного потенциала. Поддержание уровня калия > 4,5 ммоль/л и магния > 2,0 мг/дл снижает частоту желудочковых нарушений ритма и уменьшает количество эпизодов фибрилляции предсердий на 25%.
Инфузия сульфата магния, особенно в первые 24 часа послеоперационного периода, доказала эффективность в снижении риска желудочковой тахикардии и аритмий re-entry на 22%, особенно у пациентов с пролонгированным ИК.
Минимизация времени искусственного кровообращения (ИК) и времени пережатия аорты – один из ключевых организационных факторов. Снижение длительности ИК на каждые 10 минут уменьшает риск аритмий на 3–5%. При этом общая эффективность стратегий управления временем операции оценивается в 15%.
Интраоперационное наложение временного эпикардиального электрокардиостимулятора у пациентов с риском АВ-блокады и после вмешательств на клапанах способствует раннему контролю ритма и профилактике тяжёлых форм брадикардии и блокад. Эффективность достигает 18% при правильном выборе показаний.
Ниже представлена диаграмма, отражающая сравнительную эффективность различных профилактических методов (рис. 2).
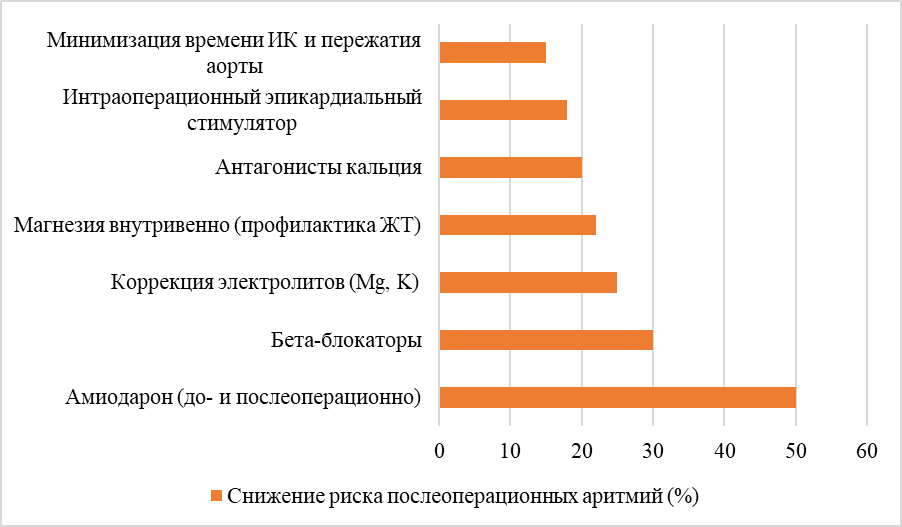
Рис. 2. Эффективность различных профилактических методов
Комплексная реализация указанных стратегий в протоколах периоперационного ведения пациентов позволяет улучшить кардиохирургические исходы и снизить бремя послеоперационной аритмогении.
Лечение послеоперационных нарушений сердечного ритма требует быстрого реагирования, основанного на характере аритмии, её гемодинамическом влиянии и прогнозе. Выбор терапевтической тактики должен учитывать особенности пациента, хирургическое вмешательство и рекомендации международных клинических руководств [4, с. 35].
Основные принципы лечения включают:
- стабилизацию гемодинамики, если аритмия приводит к ухудшению кровообращения;
- купирование аритмии, при необходимости с использованием антиаритмических препаратов или электроимпульсной терапии;
- профилактику рецидивов с учётом механизма нарушения ритма.
Особое внимание уделяется выбору антиаритмических препаратов. Амиодарон остаётся препаратом первой линии при ФП и ЖТ в послеоперационном периоде за счёт низкой проаритмогенности. Лидокаин используется при желудочковых аритмиях, особенно связанных с ишемией. При брадикардии и блокадах – временная электрокардиостимуляция (ЭКС) предпочтительна до стабилизации состояния.
Кардиоверсия – как медикаментозная, так и электрическая – применяется при нестабильных или персистирующих формах ФП, трепетания предсердий и ЖТ. При рефрактерных аритмиях, устойчивых к терапии, возможно проведение радиочастотной абляции (РЧА) в позднем послеоперационном периоде.
На рисунке 3 представлена частота применения различных методов лечения послеоперационных аритмий.
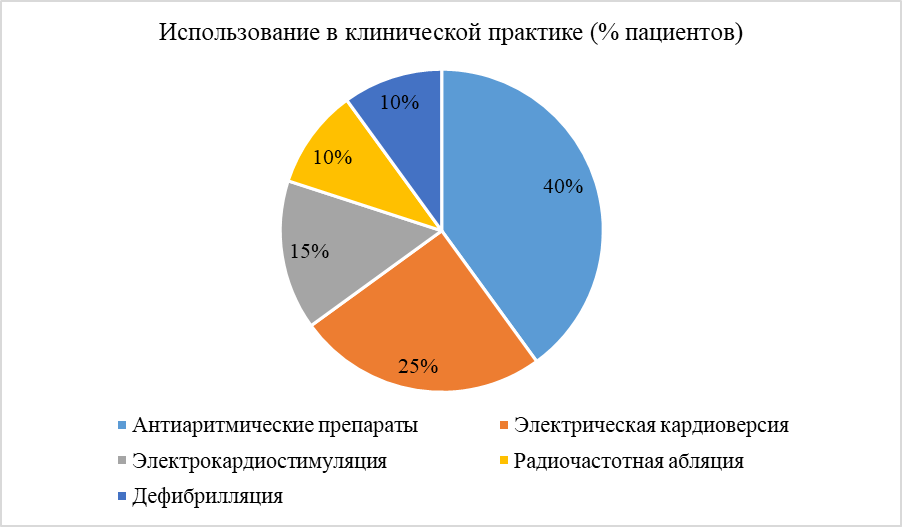
Рис. 3. Частота применения различных методов лечения послеоперационных аритмий
Тактика лечения должна быть частью мультидисциплинарного подхода, с участием кардиолога, анестезиолога и кардиохирурга, особенно в сложных клинических случаях. Внедрение стандартизированных протоколов и динамический мониторинг позволяют повысить эффективность лечения и снизить летальность, связанную с тяжёлыми аритмиями.
Нарушения сердечного ритма, возникающие в послеоперационном периоде, влияют как на краткосрочные исходы, так и на долгосрочный прогноз пациентов, перенёсших кардиохирургические вмешательства. Современные исследования показывают, что наличие послеоперационных аритмий, особенно фибрилляции предсердий, ассоциировано с повышением риска инсульта, прогрессированием сердечной недостаточности и увеличением смертности в течение последующих лет.
У пациентов, перенёсших эпизоды послеоперационной фибрилляции предсердий, отмечался двукратный рост риска развития ишемического инсульта в течение первых трёх лет после вмешательства. Кроме того, у 20–25% этих пациентов в течение первого года развивается персистирующая форма аритмии, требующая постоянной антикоагулянтной терапии и контроля ритма или частоты.
Желудочковые аритмии, особенно устойчивые формы, ассоциированы с более высоким риском внезапной сердечной смерти (ВСС) в отдалённом периоде, особенно при наличии сниженной фракции выброса левого желудочка (ФВ < 35%). В этих случаях показана имплантация кардиовертера-дефибриллятора (ИКД) в качестве вторичной или первичной профилактики.
Атриовентрикулярные блокады III степени, требующие постоянной электрокардиостимуляции, хоть и не увеличивают напрямую смертность, однако могут ухудшать качество жизни и способствовать диастолической дисфункции, особенно при отсутствии физиологической стимуляции с сохранением АВ-синхронности.
Прогноз также зависит от типа оперативного вмешательства. Так, после протезирования митрального клапана риск рецидива аритмий выше по сравнению с изолированным аортальным шунтированием, что связано с анатомо-функциональными особенностями левого предсердия и наличием фиброза его стенок. При этом профилактика и своевременная коррекция аритмий позволяют снизить риск осложнений и повторных госпитализаций более чем на 30%.
В отдалённой перспективе наилучшие результаты достигаются у пациентов, у которых:
- была проведена ранняя коррекция нарушений ритма;
- применялись персонализированные стратегии ведения (контроль ритма/ЧСС);
- поддерживался стабильный электролитный и гемодинамический статус;
- осуществлялось наблюдение в рамках специализированных кардио-реабилитационных программ.
Выводы
Таким образом, нарушения сердечного ритма в послеоперационном периоде остаются актуальной клинической проблемой в кардиохирургии. Их возникновение влияет на течение восстановления, длительность госпитализации и отдалённый прогноз. Ранняя диагностика, применение современных профилактических мер (включая амиодарон, коррекцию электролитов, кардиомониторинг), а также своевременное и дифференцированное лечение (кардиоверсия, электрокардиостимуляция, дефибрилляция, ИКД) позволяют снизить риск осложнений и смертности. Оптимизация тактики ведения пациентов, основанная на индивидуальной оценке риска и междисциплинарном подходе, является ключевым условием повышения качества специализированной помощи. Представленные в статье подходы подтверждают необходимость обновления клинических протоколов с учётом современных научных данных.

.png&w=640&q=75)