Применению природных минеральных сорбентов – карбонатных пород, высокодисперсных алюмосиликатов и кремнеземов, позволяющих обеспечить высокую эффективность очистки воды от нормируемых примесей ионов тяжелых металлов, посвящены работы [1–5] и других исследователей. Как показано в этих работах, основная практическая задача заключается в подборе местных материалов, имеющих невысокую стоимость, но достаточную степень очистки по отношению к извлекаемым из воды примесям. По химическому составу вода, используемая для питьевых целей, в каждом регионе имеет свои особенности, обусловленные природными факторами данной географической зоны.
В настоящей работе для исследований выбраны природные минеральные сорбенты доломит и шунгит. Их сорбционные характеристики изучены по отношению к ионам железа. Повышенное содержание ионов железа в воде, используемой для питьевых целей из подземных источников, характерно для многих регионов.
Природный доломит – осадочная карбонатная горная порода, преимущественно состоящая из породообразующего минерала класса карбонатов - доломита CaCO3·MgCO3. На основе природного доломита изготавливают фильтрующие материалы, которые обладают способностью корректировать рН очищаемой воды.
Шунгит – горная порода осадочного происхождения, по структуре представляющая собой природный углерод–углеродный композит и минералы (кварц, полевой шпат, алюмосиликаты, карбонаты, пириты). Шунгитовые породы различных месторождений подразделяются по содержанию шунгитового углерода и по составу минеральной основы (алюмосиликатной, силикатной, карбонатной). Особенностями шунгита являются химическая и каталитическая активность, возможность использования в процессах очистки и обезвреживания жидких и газообразных продуктов, бактерицидные свойства [6, 7].
Подготовка образцов к эксперименту включала измельчение дроблением, рассев по классам крупности ситовым методом. Для сорбции использовали фракцию с размером зерен 0,25-0,5 мм. Подготовленные по гранулометрическому составу природные образцы пород доломита и шунгита высушивались при комнатной температуре до воздушно-сухого состояния. В дальнейшем образцы шунгитового материала подвергались термообработке при температуре 380 оС в течение 1 часа.
Эффективность использования данных сорбентов для очистки оценивали на модельных водных растворах, приготовленных на дистиллированной воде с содержанием ионов железа(III) различной концентрации, при соотношении твердой (Т) и жидкой (Ж) фаз 1:100. Сорбцию ионов железа изучали в статическом режиме при температуре 25 оС. Процесс сорбции проводили путем смешивания сорбента с исследуемой водой, выдерживая в течение заданного времени, отделения раствора от твердой фазы фильтрованием. Использовали растворы в интервале концентраций ионов железа от 0,5 до 4 мг/дм3. Для исследования кинетики процесса сорбции использовали модельные растворы с фиксированной концентрацией ионов железа 2 мг/дм3 и 4 мг/дм3. Измерения рН растворов проводили с использованием иономера И-130М. Концентрацию ионов железа в растворе до и после сорбции определяли фотометрическим методом на фотоколориметре КФК-2МП по стандартным методикам при длине волны λ = 540 нм с использованием кюветы с толщиной поглощающего свет слоя 30 мм.
Степень извлечения ионов железа из модельных водных растворов α, %, и величину адсорбции Г, мг/г, рассчитывали по разности концентраций начальной С0 и остаточной (равновесной) Сравн в каждый данный момент времени по формулам
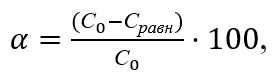
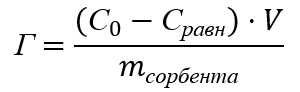
где С0 и Сравн – начальная и равновесная концентрации ионов железа, мг/дм3; V – объем исследуемого раствора, дм3; mсорбента – масса навески сорбента, г; Г – сорбционная емкость сорбента, мг/г.
Построенные зависимости изменения концентрации остаточного содержания ионов железа в растворе от продолжительности τ контакта раствора с сорбентом в координатах Сτ = f(τ) показали, что характер сорбционной активности доломита и шунгита идентичен. Наибольшие изменения в значениях остаточной концентрации ионов железа наблюдаются на начальных стадиях адсорбции в небольшом интервале первых 15 минут контакта раствора с сорбентами. Из кинетического эксперимента определено, что продолжительность адсорбции в течение 90 мин является достаточной для установления равновесия в системе. Дальнейшее увеличение продолжительности контакта раствора с сорбентами не приводит к существенному изменению концентрации определяемых ионов железа в растворе. В условиях выполненного эксперимента установлено, что природный шунгит по сравнению с доломитом имеет более низкую адсорбционную емкость по отношению к ионам железа. С учетом известных данных о термостойкости материала, в настоящей работе далее исследования проводили с образцом шунгита, термически обработанным при температуре 380 оС в течение 1 часа, что обеспечивает удаление гигроскопической и физически связанной воды из структуры минерала и способствует увеличению объема пор и удельной поверхности. Потеря массы образца шунгита в таком режиме термообработки составила 1,98 мас.%.
Изучение равновесия адсорбции ионов железа из растворов проводили в интервале концентраций 0,5 - 4 мг/дм3. Продолжительность адсорбции, необходимую для установления сорбционного равновесия между сорбентом и извлекаемыми ионами железа, выдерживали в течение 90 мин. В условиях установившегося равновесия в системе рассчитывали равновесную сорбционную емкость сорбента Гравн по иону железа. Для исследованных природных материалов было установлено, что содержание ионов железа в воде в рассматриваемом диапазоне исходных концентраций в результате сорбции термически модифицированным шунгитом снижается в 6,1 – 15,8 раз, тогда как для природного шунгита этот показатель определялся в пределах 2,6 – 7,3 раз. В опытах с природным доломитом снижение концентрации ионов железа в исследованном диапазоне исходных концентраций определяется значениями 3,7 – 14,6 раз, близкими по этому показателю термически модифицированному шунгиту. Степень извлечения ионов железа при использовании доломита и термически модифицированного шунгита составляла более 90 %, остаточная концентрация ионов железа не превышала установленные нормативы для состава питьевой воды (ПДКFe=0,3 мг/дм3) [8]. С использованием необработанного природного шунгита непревышение ПДК по содержанию ионов железа в растворе установлено при их содержании в очищаемой воде в пределах концентраций до 2 мг/дм3.
Таким образом, экспериментальные исследования показали, что доступные для многих регионов природные доломит и термически модифицированный шунгит по величине адсорбционной способности по отношению к ионам железа характеризуются близкими значениями и являются эффективными сорбентами.

