Удаление водорастворимых солей из паст азопигментов методом декантации, повышение их колористической концентрации на стадии отмывки водами различной кластерной структуры достигается введением нано-структурированных материалов.
Метод удаления водорастворимых солей из паст азопигментов структурированной водой позволяет использовать отработанные промывные воды с третьей стадии процесса декантации повторно, что ведет к сокращению количества потребляемой воды в 4 раза по сравнению с промывкой на фильтрах до заданной концентрации водорастворимых солей в пасте пигмента, что позволяет снизить потребление промывной воды в 1,47 раза, затраты на электроэнергию в 2,7 раза.
Для обеспечения высокой степени очистки паст пигментов от хлористых солей необходимо создать воду с высокой растворимостью NaCl, что обеспечит получение органических пигментов с качественным характеристиками выше нормативных.
Растворимость солей NaCl в воде различной кластерной структуры
Растворимость – способность вещества образовывать с другими соединениями однородные системы – растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц, которая для твердых солей зависит от температуры, и кластерной структуры растворителя. Момент, при котором в растворе, растворённое вещество при данных условиях достигло максимальной концентрации и больше не растворяется, является моментом насыщения.
Определение растворимости солей в растворителе
Растворимость соли в водах различной кластерной структуры определяли по показанию электрической проводимости. Для этого вначале брали воды с разными структурами, далее измеряли показатели электрической проводимости каждой воды поддерживая температуру 20 0С с помощью криостата / термостата ТЖ–ТС–01. Затем порциями добавляли соль (NaCl), при постоянном перемешивания, и измеряли удельную электрическую проводимость. Процесс ввели до тех пор, пока показатель электрической проводимости не начинал падать вследствие того, что по мере насыщения раствора электролитом (солью) усиливается электростатическое взаимодействие между ионами.
Растворимость солей (NaCl) в воде различной кластерной структуры
Концентрация соли (NaCl) в водах различной кластерной структуры и электрическая проводимость этих вод представлены в таблице 1.
Анализ полученных значений по содержанию соли (NaCl) в водах (таблица 1) показывает, что солесодержание вод различно и зависит от их кластерной структуры.
Таблица 1
Концентрация соли (NaCl) в водах различной кластерной структуры
Измеримый показатель | Тип структуры воды | |||
Артезианская вода | Дистиллированная вода | Талая дистиллированная вода | Дистиллированная вода, пропущенная через УСВР | |
| Электрическая проводимость воды, мкСм/см | 727 | 5,2 | 8,79 | 12,2 |
| Содержание NaCl (г) на 100 мл H2O | 0,00635 | 0,00011 | 0,00018 | 0,00021 |
Значения величин растворимости соли в водах различной кластерной структуры, при температуре 20 0С, представлены, в таблице 2 и на рисунке 1.
Таблица 2
Растворимость солей в воде различной кластерной структуры при температуре 20 0С
Измеримый показатель | Тип структуры воды | |||
Артезианская вода | Дистиллированная вода | Талая дистиллированная вода | Дистиллированная вода, пропущенная через УСВР | |
| Электрическая проводимость воды, мкСм/см | 43700 | 51778 | 60803 | 57460 |
| Концентрация NaCl (г) на 100 мл H2O | 30,4 | 35,2 | 35,0 | 34,9 |
На рисунке 1 представлена зависимость электрической проводимости вод различной кластерной структуры от количества растворенного (концентрации) сильного электролита – NaCl, характеризующаяся наличием максимума. Для сильных электролитов с ростом концентрации увеличивается число ионов в единице объема, и сначала наблюдается увеличение электрической проводимости. Однако при дальнейшем возрастании концентрации увеличение вязкости раствора и взаимодействия между ионами приводят к снижению скорости движения ионов и соответственно электрической проводимости.
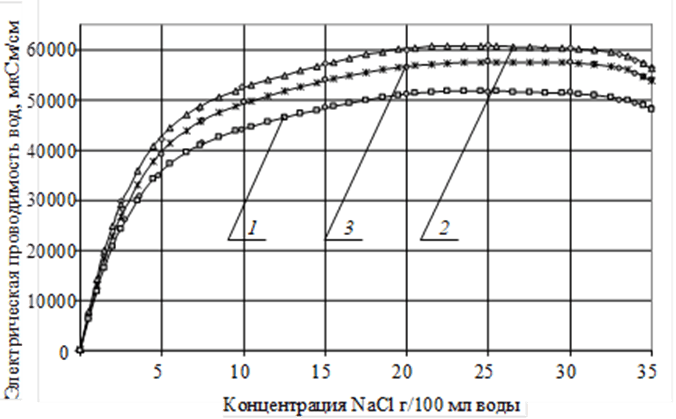
Рис. 1. Электрическая проводимость вод различной кластерной структуры в зависимости от количества соли (NaCl), вводимой в растворитель:
1 – дистиллированная вода; 2 – талая дистиллированная вода;
3 – дистиллированная вода, пропущенная через УСВР
Растворимость соли (NaCl) в воде различной кластерной структуры при наличии в них материалов в наноструктурированной форме
Растворимость соли в водах различной кластерной структуры при наличии материалов в наноструктурированной форме определяли по показанию электрической проводимости. Брали воды с разными структурами, измеряли показатели электрической проводимости каждой воды как с введенными наноматериалами, так и без них. Затем порциями добавляли соль (NaCl), при постоянном перемешивания, и измеряли удельную электрическую проводимость. Процесс ввели до тех пор, пока показатель электрической проводимости не начинал падать и соль не переставала растворяться.
Экспериментальные исследования по определению растворимости соли (NaCl) в воде различной кластерной структуры при наличии металлов в наноструктурированной форме представлены на графических зависимостях при наличии наноматериалов (Cu, Ni, Fe).
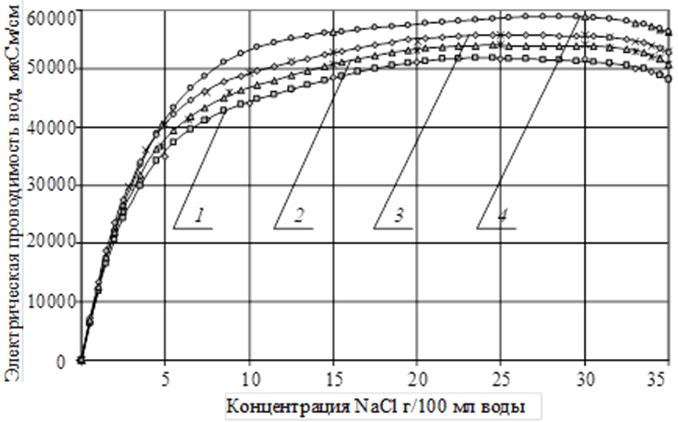
Рис. 2. Электрическая проводимость дистиллированной воды в зависимости от концентрации соли (NaCl), вводимой в растворитель в присутствии наноматериалов:
1 – дистиллированная вода; 2 – дистиллированная вода с нано –Fe;
3 – дистиллированная вода c нано –Cu; 4 – дистиллированная вода с нано –Ni
На рисунке 2 представлены зависимости электрической проводимости дистиллированной воды от концентрации соли (NaCl), вводимой в воду в присутствии наноматериалов Fe, Cu, Ni. Характер представленных кривых свидетельствует о том, что дистиллированная вода растворяет максимум соли (NaCl) при введении нанометала Ni, далее по растворимости идет Fe и Cu, наименьшее количество соли растворяется в обычной дистиллированной воде без ввода наноматериалов. Экспериментальные результаты подтверждают факт увеличения предела насыщаемости дистиллированной воды солью NaCl при введении нанометаллов Ni, Fe, Cu.
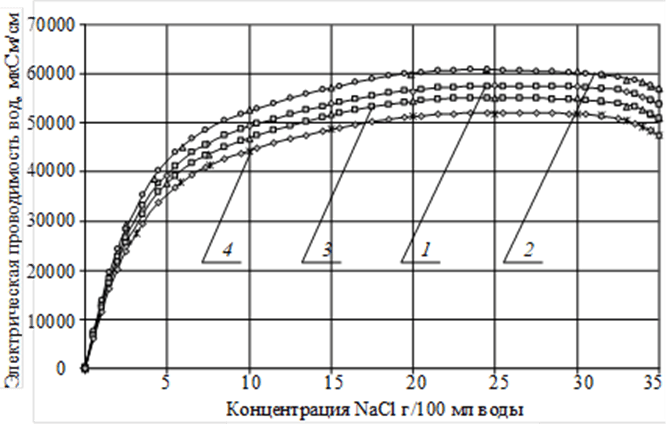
Рис. 3. Электрической проводимость дистиллированной воды пропущенной через УСВР в зависимости от концентрации соли (NaCl) вводимой в растворитель в присутствии нанометаллов:
1 – дистиллированная вода, пропущенная через УСВР;
2 – дистиллированная вода, пропущенная через УСВР с нано –Fe;
3 – дистиллированная вода, пропущенная через УСВР c нано –Cu;
4 – дистиллированная вода, пропущенная через УСВР с нано –Ni
Зависимости представленные на рисунке 3 свидетельствуют, что у дистиллированной воды пропущенной через УСВР максимальное значение растворимости соли (NaCl) достигается при введении нано–Fe, далее непосредственно в самой дистиллированной воде пропущенной через УСВР и при введении нано-Cu и Ni. Следовательно, максимальная растворимость соли (NaCl) достигается при введении в дистиллированную воду, пропущенную через углерод высокой реакционной способности (УСВР) нано-Fe.
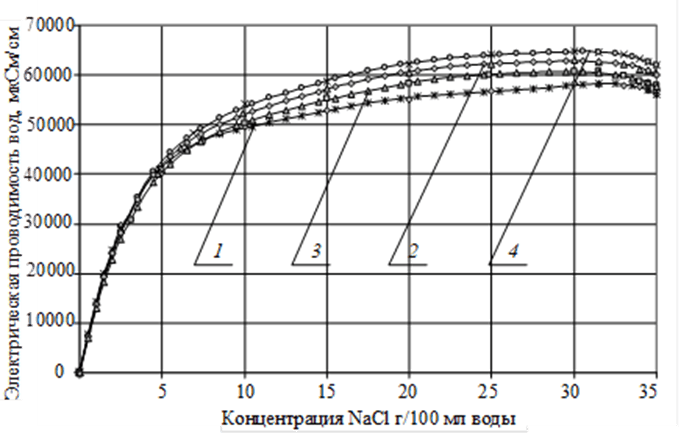
Рис. 4. Электрическая проводимость талой дистиллированной воды в зависимости от концентрации соли (NaCl), вводимой в растворитель в присутствии нанометаллов:
1 – талая дистиллированная вода; 2 – талая дистиллированная вода с нано –Fe;
3 – талая дистиллированная вода с нано –Сu;
4 – талая дистиллированная вода с нано –Ni
Из анализа представленных зависимостей можно сделать вывод на рисунке 4, что талая дистиллированная вода растворяет максимум соли (NaCl) при введении нанометалла Ni, далее по растворимости идет Fe и Cu, наименьшее количество соли растворяется в обычной талой дистиллированной воде без ввода нанометаллов.
Следовательно, из зависимостей представленных на рисунках 2–4 следует, что дистиллированная, талая дистиллированная воды растворяют максимальное количество соли (NaCl) при введении нанометалла Ni. Тогда как дистиллированная вода, пропущенная через УСВР – при введении нанометалла Fe.
Выводы
Из результатов, представленных на рисунках 1-4 следует, что при ведении нанометаллов Ni, Fe и Cu максимальная растворимость характерна для дистиллированной воды, пропущенной через УСВР, а при введении нанометала Fe максимум растворения достигается для талой дистиллированной воды. Для обеспечения высокой степени очистки пигментов и красителей от водорастворимой соли NaCl, необходимо формировать растворитель со структурой талой дистиллированной воды с вводом наноматериалла Ni.

