Введение
АИГ определяется как хроническое заболевание печени, которое может поразить любого человека в любом возрасте. Оно встречается преимущественно у женщин (70-80%), соотношение женщин и мужчин составляет 4:1-10:1. Заболевание может поражать людей любого возраста, пик заболеваемости приходится на возраст 10-30 лет и 45-70 лет [2]. Последние эпидемиологические исследования указывают на тенденцию к увеличению распространенности ВГА во всем мире, особенно среди пациентов мужского пола, эта тенденция может свидетельствовать об изменении пусковых факторов в возникновении заболевания с течением времени [4].
Течение заболевания иногда может быть флуктуирующим (непостоянным), но в целом прогрессирующим.
В 25% случаев АИГ развивается бессимптомно и выявляется на стадии цирроза печени, что диктует необходимость активного скрининга этих пациентов. Внепеченочные проявления часто негативно влияют на прогрессирование заболевания и ответ на лечение. Согласно последним научным данным, 40% пациентов с неконтролируемым тяжелым заболеванием печени умирают в течение шести месяцев после выявления заболевания. У остальных пациентов с НАС развивается прогрессирование тяжелых заболеваний печени, таких как цирроз печени и пищеводные кровотечения из-за варикозного расширения вен пищевода. В острых клинических случаях АИГ может проявляться в виде энцефалопатии в течение 8 недель [3].
Существует множество форм сочетания АИГ с другими заболеваниями, особенно с сопутствующими холестатическими патологиями, такими как первичный билиарный холангит (ПБХ) или первичный склеротический холангит (ПСХ). Диагностика также требует исключения других причин гепатита, таких как токсический лекарственный гепатит, вирусный гепатит, алкогольный гепатит или неалкогольный стеатогепатит, поскольку некоторые из этих заболеваний реагируют на иммуносупрессивную терапию.
Лечение длительное, не менее 3 лет, но часто может быть пожизненным, со многими побочными эффектами и недостаточным ответом на текущие лекарства. Лечение АИГ является серьезной проблемой после 50 лет усилий и испытаний. Даже в настоящее время она остается научной проблемой для диагностики и лечения. Тем не менее, это было первое заболевание печени, для которого применение кортикостероидов было убедительно доказано в клинических контрольных испытаниях [1].
Объекты и методы исследования
Для проведения данного исследования был разработан план исследования, ориентированный на определение целей и задач. Клинический материал был отобран на базе гепатологических отделений ИМСП Республиканской клинической больницы "Тимофей Мошнеага", период 2019–2022 гг.
Исследование кросс-секционное, смешанное (ретроспективное и проспективное), основано на анализе данных, внесенных в листы наблюдения за пациентами информационной системы здравоохранения больницы (SIAAMS) и клиническом обследовании пациентов, включенных в исследование.
Установление объекта исследования позволило определить критерии включения и исключения исследуемой популяции. Был составлен перечень характеристик, используемых для определения права на включение в исследование.
Критерии включения
Пациенты с ХАИ, диагностированным в соответствии с критериями, предложенными Международной группой по изучению аутоиммунного гепатита (IAIHG).
Критерии исключения:
- Гепатит другой этиологии.
- Вирусные гепатиты B,C,D, вирус Эпштейна-Барр, цитомегаловирус, HAV.
- Алкогольный гепатит
- Лекарственно-индуцированное поражение печени.
- Гранулематозный гепатит
- Метаболически ассоциированный стеатогепатит
- Гемохроматоз
- Болезнь Вильсона
Протокол исследования включает:
1. Общая информация: возраст, пол, тип АИГ
2. Полный личный анамнез: сопутствующие заболевания, наличие вирусного гепатита, наличие цирроза печени.
3. Клинические особенности на основании следующих клинических симптомов и синдромов:
- Астеновегетативный синдром, который включал симптомы нервно-психической астении, головокружения, головной боли различной локализации, утомляемости.
- Абдоминальный болевой синдром, проявляющийся болью различной интенсивности с локализацией в правом подреберье или в эпигастрии.
- Диспепсический синдром, характеризующийся постпрандиальной полнотой в эпигастрии, потерей аппетита, изжогой тошнотой, рвотой, метеоризмом, запорами или стулом полуоформленный стул.
- Гепатомегалия, определяемая пальпаторно, когда нижняя граница печени расположена более чем на 2 см ниже костального края.
- Спленомегалия – увеличение селезенки, превышающее пределы физиологических изменений.
- Суставной синдром, проявляющийся болью, трещанием и дискомфортом в суставах.
- Желтуха, представляющая собой желтое обесцвечивание кожи, склер и слизистых оболочек пациента, вызванное их пропитыванием желчными пигментами (билирубином), находящимися в избытке в кровеносной системе.
- Недомогание, приводящее к потере веса.
4. Анализ лабораторных методов
Результаты и их обсуждение
Клинический материал был отобран на базе отделения гепатологии ИМСП Республиканской клинической больницы "Тимофей Мошнеага" Кишинев, в течение 2019-2022 гг. Для проведения диссертационного исследования мы использовали информацию, собранную у пациентов и лист клинического наблюдения. В исследуемой группе был обследован 21 пациент с аутоиммунным гепатитом из разных населенных пунктов республики: 90,5% (19) женщин и 9,5% (2) мужчин; из них 33,4% (7) в возрасте до 40 лет и 66,6% (14) - старше 40 лет, средний возраст составил 51,65 лет (рис. 1).
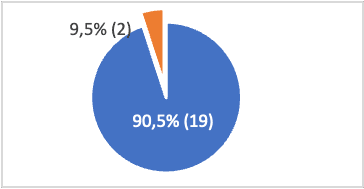
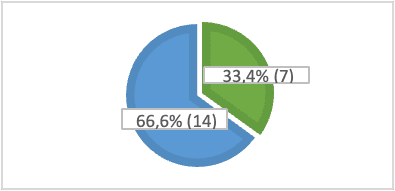
Рис. 1. Распределение пациентов по полу и возрасту
Контрольную группу составили 20 практически здоровых лиц 44,2% (9) мужчин и 55,8% (11) женщин, без отягощенного наследственного анамнеза, при отсутствии патологии печени и желудочно-кишечного тракта.
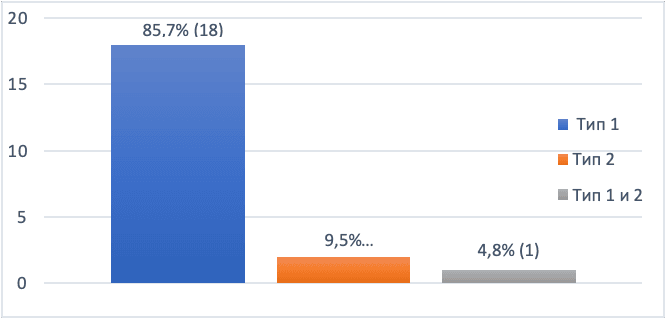
Рис. 2. Распределение пациентов исследуемой группы по типам ВГА
Результаты: ANA – положительный у 16 пациентов, что составляет 76,1%; Antip-ANCA – 23,8% (положительный у 5 пациентов); ASMA – 19% (положительный у 4 пациентов); AntiLKM1 – 9,5% (положительный у 2 пациентов); AntidsDNA – 14,2% (положительный у 3 пациентов); AMA – 19% (положительный у 4 пациентов). У одного из пациентов были обнаружены положительные антитела ANA и Anti-LKM1, поэтому мы отнесли этого пациента к смешанному типу АИГ (тип 1 и тип 2). Графическое представление результатов представлено на рис.2 и рис.3.
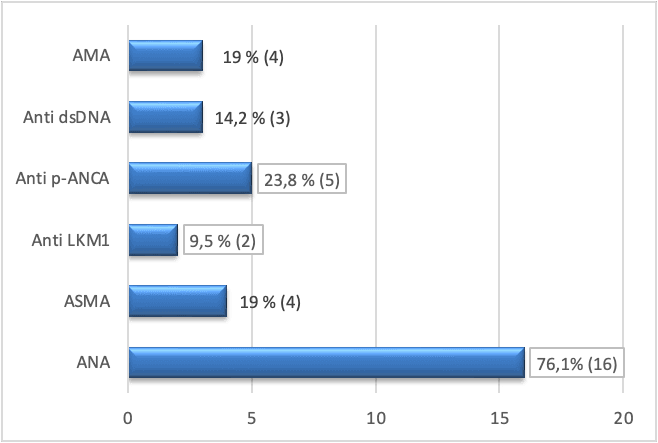
Рис. 3. Частота встречаемости аутоиммунных маркеров и органных неспецифических антител в исследуемой группе
Заключение. Высокая частота встречаемости ANA (76,1%) в исследуемой группе согласуется с литературными данными, которые показывают наличие ANA у 90% пациентов с аутоиммунным гепатитом.
Тщательное обследование пациентов выявило наличие сопутствующих заболеваний, среди которых преобладали следующие: реактивный артрит 23,8% (5), гастроэзофагеальная рефлюксная болезнь 33,3% (7), синдром раздраженного кишечника 9,5% (2), эритематозная гастродуоденопатия 33,3% (7), первичный билиарный цирроз 9,5% (2) , вирусный гепатит С 14,2% (3), вирусный гепатит В 14,2% (3), синдром суперинфекции 23,8% (5), включая 4 пациентов с первичным билиарным холангитом и 1 пациента с первичным склерозирующим холангитом. Из внепеченочных аутоиммунных состояний, ассоциированных с НАСГ, аутоиммунный тиреоидит был выявлен в 61,9% (13), а синдром Шогрена – в 14,2% (3).
Оценка эффективности лечения ХАИ по клиническим синдромам
Из исследуемой группы 16 пациентам проводилось иммуносупрессивное лечение, из них 10 (62,5%) – монотерапия преднизолоном (по схеме лечения 60-40 мг вначале со снижением дозы до 15-10 мг/сут), а в комбинированной схеме преднизолон + азатиоприн – 6 пациентов (37,5%). В гепатологическом отделении Республиканской клинической больницы ИМСП пациентам с АИГ проводилось иммуносупрессивное лечение и этиопатогенетическая терапия.
Для оценки эффективности иммуносупрессивной терапии синдромы и симптомы, выявленные у пациентов с АИГ, оценивались до и после терапии (табл. 1.).
Таблица 1
Эволюция клинических синдромов и симптомов при АИГ до и после иммуносупрессивной терапии
|
Клинические синдромы и симптомы |
При поступлении |
При выписке |
|---|---|---|
|
Астеновегетативный синдром |
100% (16) |
50% (8) |
|
Абдоминальный болевой синдром |
56,25% (9) |
37,5% (6) |
|
Диспепсический синдром |
50% (8) |
37,5% (6) |
|
Гепатомегалия |
87,5% (14) |
56,25% (9) |
|
Спленомегалия |
68,75% (11) |
50% (8) |
|
Суставной синдром |
43,75% (7) |
18,75% (3) |
|
Желтуха |
62,5% (10) |
25% (4) |
|
Потеря веса |
18,75% (3) |
12,5% (2) |
Иммуносупрессивная терапия оказала благоприятное влияние на эволюцию клинических синдромов. У пациентов отмечался истинный регресс клинических синдромов: астеновегетативного (p<0,01), тоскливого (p<0,01), спленомегалии (p<0,01), суставного (p<0,05) и желтухи (p<0,05). Также определялась тенденция к улучшению других клинических проявлений.
Лабораторные данные
Цитолитический синдром. Активность АЛТ и АСТ определяли до и после терапии HAI. У пациентов контрольной группы значения АЛТ и АСТ находятся в пределах нормы, 25,44±1,10 Ед/л и 18,12±1,44 Ед/л.
У пациентов II группы, представленной пациентами до начала иммуносупрессивной терапии, сравнительный анализ аминотрансфераз в группах II и III, выявил более низкие значения АЛТ на 2,1 и АСТ на 2,3, что указывает на положительный ответ до лечения p<0,05. которые, однако, оставались высокими по сравнению с показателями контрольной группы в 2,7 раза (табл. 2).
Таблица 2
Оценка эффективности иммуносупрессивной терапии на цитолитический синдром у пациентов с ВГА
|
показатели |
группы значения – I |
II |
III |
p II–III |
|
АЛТ U/l |
25,44±1,10 |
148,12± 30,14** |
65,35± 12,13 |
p<0,05 |
|
AСT U/l |
18,12±1,44 |
135,14± 34,25** |
60,11± 10,12 |
p<0,05 |
Примечание: *-p<0,05; **p<0,01: ***p<0,001 – разница между I и II партиями
Иммунно-воспалительный синдром. В контрольной группе значения показателей гуморального иммунитета находятся в пределах нормы: Ig A – 2,34±0,15 (г/л), Ig M - 1,5±0,08(г/л), Ig G – 11,02±0,21(г/л), ЦИК - 95±7,23(УДО).
При АИГ уровни IgA, IgM, Ig G и ЦИК были статистически достоверно выше по сравнению с контрольной группой (p<0,001), что свидетельствует в пользу того, что при ХАИ преобладает иммуновоспалительный синдром.
Выводы
- При клинической оценке пациенток в исследуемой группе мы отметили преобладание АИГ у женщин молодого возраста, средний возраст составил 41,65 лет, что соответствует литературным данным.
- Оценка сопутствующих патологий у пациентов с аутоиммунным гепатитом выявила более частое наличие аутоиммунного тиреоидита, суставного синдрома, синдрома Согрена, а у 25% было выявлено перекрытие синдрома аутоиммунного гепатита с ХБП или ХПН.
- Гуморальные иммунологические изменения характеризуются преимущественным повышением IgG у пациентов с аутоиммунным гепатитом по сравнению со здоровыми лицами, а исследование специфических аутоантител выявило преобладание антител ANA, затем ASMA у пациентов с АИГ.
- У пациентов с аутоиммунным гепатитом во время иммуносупрессивной терапии наблюдалось достоверное снижение трансаминаз по сравнению с исходным уровнем (p<0,05) и значительное снижение IgG, что прогнозирует эффективность иммуносупрессивной терапии.

.png&w=640&q=75)