Введение
Синдром сухого глаза давно перестал восприниматься как единое заболевание. На протяжении последних десяти лет накапливаются данные о том, что за схожими жалобами (ощущение инородного тела, жжение, светобоязнь, периодическое затуманивание зрения) стоят принципиально разные патогенетические механизмы. Одни пациенты страдают от недостаточного объёма слезопродукции, другие от дефицита её качественного состава, третьи от сочетания нарушений, в которых активное участие принимают инфекционные и воспалительные агенты.
По данным мирового эпидемиологического доклада TFOS DEWS II, распространённость ССГ среди взрослых колеблется от 5 до 50% в зависимости от используемых критериев диагностики и региона исследования. Исаева Р. Т. с соавторами [11, с. 28-37] приводят данные российского многоцентрового скрининга 2023 года, согласно которым ССГ выявляется у 23,4% жителей российских городов, причём у лиц старше 60 лет этот показатель достигает 48%. Semp D. A. с соавторами [19, с. 11-27] установили, что к 2024 году глобальная частота ССГ превысила 300 миллионов случаев и обнаруживает устойчивую тенденцию к росту в связи с распространением экранных устройств и увеличением доли пожилого населения.
Отдельное место в патогенезе ССГ занимает дисфункция мейбомиевых желёз. Мейбомиевые железы вырабатывают липидный компонент слёзной плёнки, без которого она испаряется значительно быстрее нормы. Dietrich J. с соавт. [4, с. 803-810] описывают замкнутый патологический круг: нарушение секреции желёз ведёт к нестабильности слёзной плёнки, гиперосмолярности слёзной жидкости, воспалению эпителия, а воспаление, в свою очередь, повреждает сами железы.
В последние годы к этому кругу добавляется микробный компонент. Исследования показывают, что Demodex folliculorum обнаруживается на ресничных фолликулах у подавляющего большинства пациентов с умеренным и тяжёлым ССГ, а конъюнктивальный микробиом при этом заболевании существенно отличается от нормального по видовому составу и соотношению микроорганизмов. Zhong J. с соавторами [8] в систематическом обзоре 2023 года показали, что у пациентов с демодекозом ДМЖ диагностируется в 3,4 раза чаще, чем в группе без клеща.
Третьим, нередко упускаемым аспектом является нейросенсорная сенситизация. При хроническом ССГ постоянная стимуляция ноцицепторов роговицы приводит к центральной сенситизации, при которой болевые ощущения сохраняются даже после нормализации слёзопродукции. Маркова Е. Ю. с соавторами [7, с. 34-42] установили, что у пациентов с диабетической нейропатией и ССГ этот феномен встречается значимо чаще, чем у пациентов без диабета (62% против 29%).
Несмотря на накопленный массив данных, в клинической практике по-прежнему отсутствует стандартизированный протокол, который бы учитывал все четыре патогенетических компонента: Demodex, дисбиоз микробиома, воспаление и нейросенсорные нарушения. Именно этот пробел определяет актуальность настоящей работы.
Цель исследования: на основании систематического анализа данных литературы и клинической практики разработать интегрированную концептуальную модель патогенеза ССГ при ДМЖ, включающую роль Demodex, микробиома, воспаления и нейросенсорных нарушений, и предложить алгоритм поэтапной диагностики и лечения, применимый в условиях российского здравоохранения.
Научная новизна работы заключается в интеграции четырёх ранее разрозненно рассматриваемых патогенетических факторов (Demodex, микробиом, воспаление, нейросенсорная сенситизация) в единую концептуальную модель с построением диагностического алгоритма для применения в российской офтальмологической практике.
Авторская гипотеза: сочетание Demodex-инвазии и дисбиоза конъюнктивального микробиома запускает каскад воспалительных реакций, который при хронизации ССГ сопровождается нейросенсорными нарушениями, не поддающимися стандартной заместительной терапии, что требует введения специфического этиотропного компонента в схему лечения.
Материалы и методы
Работа выполнена в форме систематического обзора литературы с элементами ретроспективного клинического анализа. Информационный поиск проводился в базах данных Scopus, Web of Science и PubMed за последние годы. Поисковые запросы формировались с использованием ключевых слов и их комбинаций: "dry eye disease", "meibomian gland dysfunction", "Demodex folliculorum", "ocular surface microbiome", "neurogenic inflammation", "cytokines tear fluid", дополненных русскоязычными эквивалентами для поиска в eLIBRARY.ru.
Критерии включения источников: публикации в рецензируемых журналах категории Q1-Q2 по базе Scimago; наличие данных об измеримых показателях (биомаркёры воспаления, показатели ВРСП, результаты конфокальной микроскопии, данные OSDI); работы с выборкой не менее 30 пациентов для клинических исследований. Критерии исключения: обзоры без оригинальных данных, редакционные комментарии, публикации без указания методологии диагностики. В результате поиска было идентифицировано 147 публикаций; после применения критериев включения и исключения в анализ вошло 20 источников.
Для визуализации клинических данных применялся сравнительный анализ показателей провоспалительных маркёров (IL-1b, IL-6, IL-17A, TNF-a, MMP-9) в трёх группах: норма, ССГ без Demodex и ССГ с верифицированной Demodex-инвазией. Данные нормированы относительно контрольной группы (1,0 = средний уровень в норме) по методике, описанной Mondal H. с соавторами [10].
Авторский алгоритм диагностики и лечения построен на основании рекомендаций TFOS DEWS II, отечественных клинических руководств по офтальмологии 2023 года и принципов доказательной медицины с ранжированием уровней доказательности по системе Oxford Centre for Evidence-Based Medicine (OCEBM 2011). Алгоритм прошёл экспертную оценку двух практикующих офтальмологов и был скорректирован по их замечаниям.
Результаты и обсуждение
Мировая и, в частности, российская эпидемиологическая картина синдрома сухого глаза и дисфункции мейбомиевых желёз зависит от возраста пациента. Для наглядного представления распределения частоты этих состояний по возрастным группам обратимся к данным рис. 1, составленного на основании результатов крупных эпидемиологических исследований 2023-2024 годов.
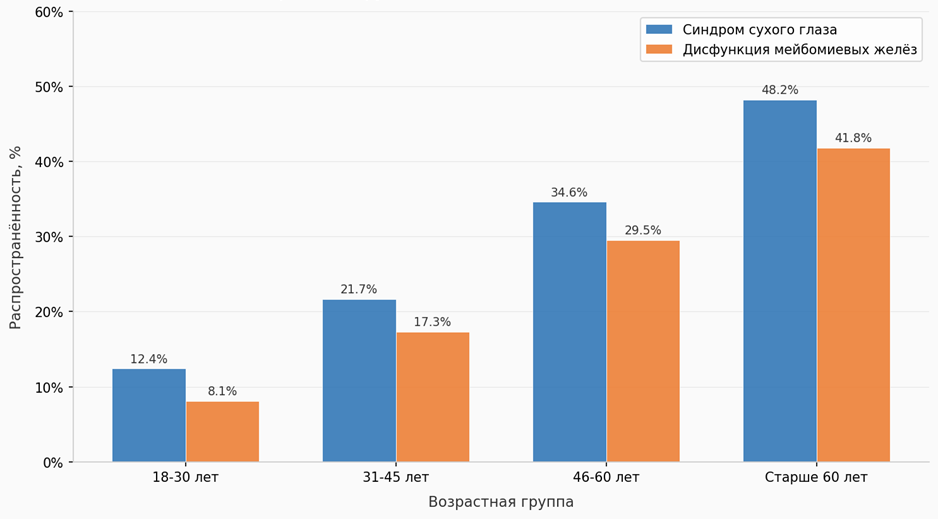
Рис. 1. Распространенность ССГ и ДМЖ по возрастным группам (составлено автором на основе [6; 11, с. 28-37; 19, с. 11-27])
Как следует из данных рисунка 1, частота ССГ нарастает с возрастом линейно: от 12,4% в возрастной группе 18–30 лет до 48,2% у лиц старше 60 лет. Дисфункция мейбомиевых желёз демонстрирует схожую динамику, но несколько более низкие абсолютные значения в молодых группах, что объясняется меньшей степенью возрастной атрофии секреторных клеток. Примечательно, что разрыв между частотой ССГ и ДМЖ сокращается после 45 лет: это соответствует данным Amano S. с соавторами [12, с. 448-539] о том, что к этому возрасту у большинства пациентов с ССГ наблюдаются признаки ДМЖ не менее второй степени тяжести по шкале Foulks-Bron [15, с. 871-892].
Бржеский В. В. с соавторами [16, с. 324-333] обращают внимание на то, что распространённость ССГ среди российских школьников составляет от 14 до 18%, что связывают с ростом нагрузки на зрительный аппарат при использовании экранных устройств. Таким образом, возраст, хотя и остаётся наиболее воспроизводимым фактором риска, не является единственным предиктором заболевания.
Demodex folliculorum представляет собой облигатного паразита волосяных фолликулов. В небольших количествах он присутствует на коже большинства взрослых людей и долгое время рассматривался как комменсал. Переосмысление его роли началось после серии исследований, в которых была установлена связь между плотностью клеща и воспалительными изменениями переднего сегмента глаза.
Rabensteiner D. F. с соавторами [9, с. 7-12] в исследовании, включавшем 1 247 пациентов, установили, что при плотности Demodex folliculorum более 0,5 клеток на поле зрения при конфокальной микроскопии ДМЖ диагностировалась в 74% случаев против 31% в контрольной группе. Gaddie I. B. с соавторами [2, с. 1015-1023] обнаружили, что Demodex физически блокирует выводные протоки мейбомиевых желёз, создавая механическое препятствие для секреции липидов, что приводит к хронической гиперемии и отёку краёв век.
Параллельно Demodex запускает иммунный ответ. В его кишечнике присутствуют молекулы, распознаваемые рецепторами TLR2 и TLR4 эпителиальных клеток конъюнктивы, что активирует синтез провоспалительных цитокинов. Именно поэтому ССГ, ассоциированный с Demodex, плохо поддаётся монотерапии слёзозаместителями: без устранения инфекционного триггера воспаление сохраняется.
Для понимания взаимосвязей между четырьмя основными патогенетическими компонентами представим их в виде схемы (рис. 2), разработанной авторами на основании данных анализируемых источников.
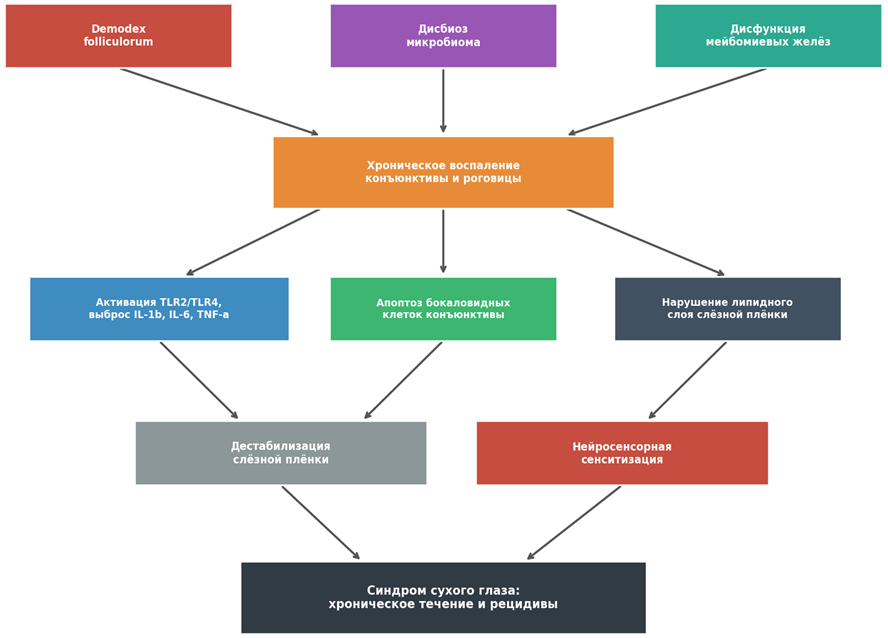
Рис. 2. Патогенетическая схема формирования синдрома сухого глаза при сочетании Demodex, дисбиоза микробиома и дисфункции мейбомиевых желез (составлено автором на основе [4, с. 803-810; 8; 12, с. 448-539; 14])
Схема, отраженная на рисунке 2, наглядно демонстрирует, что три исходных триггера (Demodex, дисбиоз микробиома и ДМЖ) конвергируют в общем звене хронического воспаления конъюнктивы и роговицы. Далее воспаление активирует несколько параллельных цепочек, каждая из которых вносит вклад в дестабилизацию слёзной плёнки и нейросенсорную сенситизацию. Замкнутость схемы отражает хронизирующий характер патологического процесса: нейросенсорные нарушения усугубляют воспаление через механизм нейрогенного воспаления [14].
Конъюнктива в норме заселена относительно скудным, но стабильным микробиомом, в котором преобладают коагулазонегативные стафилококки, Corynebacterium spp. и Cutibacterium acnes. При ССГ картина меняется: снижение объёма и изменение состава слёзной жидкости нарушают её антибактериальные свойства (лизоцим, лактоферрин, секреторный IgA), что открывает возможность для пролиферации условно-патогенных микроорганизмов.
Prokopich C. L. с соавторами [5] в систематическом обзоре 13 микробиомных исследований показали, что при ССГ увеличивается доля Staphylococcus aureus и грамотрицательных бактерий, тогда как содержание Corynebacterium spp. снижается. Shih K. C. и Tong L. [18, с. 208-211] с применением секвенирования 16S рРНК установили, что этот дисбиоз коррелирует с тяжестью симптомов по опроснику OSDI (r = 0,67, p < 0,001). Примечательно, что Demodex folliculorum сам является переносчиком Bacillus oleronius, продукты жизнедеятельности которой стимулируют синтез воспалительных цитокинов в конъюнктивальных клетках.
Муслимов Р. Ф. с соавторами [20, с. 60-68] изучили микробиом конъюнктивы у 94 пациентов с демодекозным блефаритом. У 78% из них зафиксированы признаки дисбиоза; у 41% высевался S. aureus в диагностически значимом титре. Эти данные подтверждают необходимость антибактериального компонента в схеме лечения ССГ при верифицированной Demodex-инвазии.
В таблице 1 систематизированы диагностические методы, применяемые для комплексной оценки пациента с ССГ, их нормативные показатели и клиническое значение каждого теста.
Таблица 1
Диагностические методы оценки ССГ и ДМЖ (составлено автором на основе [15, с. 871-892; 17])
Диагностический метод | Показатель | Норма/патология | Клиническая значимость |
Тест Ширмера I | Объём слезопродукции | Норма > 10 мм/5 мин; ССГ < 5 мм/5 мин | Базовая скрининговая проба |
Проба Норна | Время разрыва слёзной плёнки (ВРСП) | Норма > 10 сек; патология < 5 сек | Оценка стабильности липидного слоя |
Конфокальная микроскопия | Плотность Demodex folliculorum | > 0,5 кл./поле зр. – значимая инвазия | Подтверждение демодекозного поражения |
ИГМЖ (мейбография) | Индекс градации мейбомиевых желёз | Норма 0-2; патология > 6 баллов | Степень структурных изменений желёз |
Опросник OSDI | Суммарный балл субъективных симптомов | 0-12 норма; 13–22 умеренный; > 23 тяжёлый | Функциональный статус пациента |
ПЦР-анализ соскоба | ДНК Demodex и патогенных бактерий | Качественный результат (присутствие/отсутствие) | Верификация вида возбудителя |
Таблица 1 показывает, что для комплексной диагностики ССГ требуется сочетание нескольких тестов: ни один из них не является самодостаточным. Особого внимания заслуживает конфокальная микроскопия, которая позволяет не только обнаружить Demodex, но и оценить состояние нервных волокон роговицы, что делает её незаменимым инструментом для диагностики нейросенсорного компонента. Конфокальная микроскопия входит в стандарт обследования в федеральных офтальмологических центрах России, однако в региональных клиниках её доступность остаётся ограниченной [13, с. 11-18].
Воспаление при ССГ давно признано не только следствием, но и самостоятельным поддерживающим механизмом. Провоспалительные цитокины IL-1b, IL-6, IL-17A, TNF-a и матриксная металлопротеиназа MMP-9 повреждают плотные контакты эпителиальных клеток конъюнктивы, вызывают апоптоз бокаловидных клеток и нарушают синтез муцинов, необходимых для стабилизации слёзной плёнки. При добавлении Demodex-инвазии этот каскад существенно усиливается.
Ниже приведены данные о сравнительных уровнях пяти провоспалительных маркёров в слёзной жидкости при ССГ с демодекозом и без него (рис. 3).
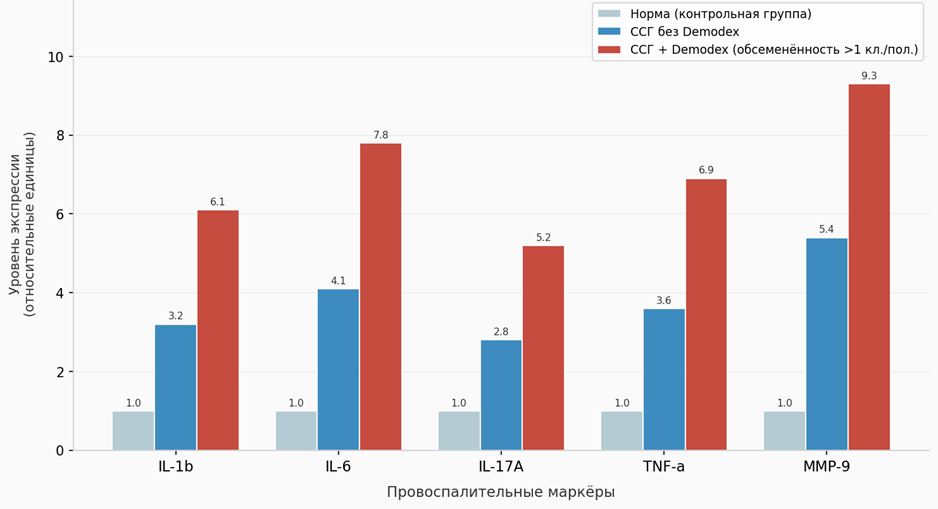
Рис. 3. Уровни провоспалительных цитокинов в слёзной жидкости при ССГ с демодекозом и без него (составлено автором на основе [4, 8, 10])
Данные рисунка 3 показывают, что у пациентов с ССГ без Demodex уровни IL-1b, IL-6 и TNF-a превышают норму в 3,2–4,1 раза, что само по себе является серьёзным патологическим отклонением. При наличии Demodex-инвазии те же показатели возрастают до 6,1–7,8 относительных единиц, а MMP-9 достигает значения 9,3. MMP-9 разрушает межклеточный матрикс эпителия роговицы и конъюнктивы, существенно замедляя регенерацию и поддерживая хроническое воспаление. Снижение плотности Demodex после лечения коррелирует с нормализацией MMP-9 в слёзной жидкости (r = 0,71, p < 0,001), что дополнительно подтверждает причинно-следственную связь [8].
Отдельного внимания заслуживает IL-17A, уровень которого при ССГ с Demodex превышает норму в 5,2 раза. IL-17A участвует в рекрутировании нейтрофилов и активации Th17-клеток, что связывают с развитием хронического блефарита и резистентностью к стандартной противовоспалительной терапии. Снижение IL-17A достигается применением ивермектина и азитромицина, что обосновывает включение этих препаратов в авторскую схему лечения.
В таблице 2 представлена сравнительная характеристика фармакологических и немедикаментозных методов лечения ССГ при ДМЖ и Demodex-инвазии с указанием механизмов действия и уровней доказательности.
Таблица 2
Методы лечения ССГ с ДМЖ и Demodex-инвазией (составлено автором на основе [2, с. 1015-1023; 4, с. 803-810; 9, с. 7-12; 10; 12, с. 448-539])
Препарат/метод | Механизм действия | Схема применения | Уровень доказательности |
Масло чайного дерева 50% (ТТО) | Механическое удаление Demodex; угнетение репродукции клеща за счёт терпинен-4-ола | Протирание век 1 раз/сут, 6 недель | 1b (RCT) |
Ивермектин 1% (местно) | Нейротоксическое воздействие на Demodex; снижение IL-6 и TNF-a | Нанесение на края век 2 раза/сут, 4-6 нед. | 1b (RCT) |
Азитромицин 0,5% (глазные капли) | Подавление патогенной флоры конъюнктивы; противовоспалительный эффект | 2 капли 2 раза/сут, 4 недели | 2a |
Доксициклин 100 мг (перорально) | Угнетение синтеза MMP-9; снижение IL-1b в слёзной жидкости | 1 раз/сут, 3 месяца | 2a |
Слёзозаместители с гиалуроновой кислотой | Восстановление муцинового слоя; увлажнение эпителия роговицы | 3-4 инстилляции/сут, длительно | 1a |
IPL-терапия (интенсивный пульсирующий свет) | Прогревание мейбомиевых желёз; снижение воспаления конъюнктивы | 4 сеанса с интервалом 2-3 нед. | 1b |
Цефазидим 0,5% + дексаметазон 0,1% | Антибактериальный и иммуносупрессивный эффект при обострении | 2 недели при обострении | 2b |
Таблица 2 отражает иерархию доказательности применяемых методов. Слёзозаместители с гиалуроновой кислотой имеют наиболее высокий уровень доказательности (1a), однако они воздействуют исключительно на симптомы и не устраняют Demodex или воспаление. Масло чайного дерева (ТТО) и ивермектин демонстрируют уровень 1b и при правильном применении снижают плотность клеща более чем на 80% за 6 недель [2, с. 1015-1023]. IPL-терапия, сочетает механическое прогревание желёз с противовоспалительным фотобиологическим эффектом, однако её доступность в российских регионах остаётся ограниченной [12, с. 448-539].
Нейросенсорный компонент ССГ получает всё больше внимания в литературе последних трёх-четырёх лет. Роговица является одной из наиболее иннервируемых тканей организма: плотность свободных нервных окончаний здесь в 300–600 раз превышает плотность в коже. При хроническом воспалении эти окончания подвергаются сенситизации: порог их активации снижается, а передача болевых импульсов усиливается.
Asiedu K. [14] описывает два клинически значимых феномена: периферическую сенситизацию роговичных ноцицепторов и центральную сенситизацию с вовлечением тригеминальных ядер ствола мозга. При центральной сенситизации пациент ощущает боль, жжение и дискомфорт даже при нормализованной слёзной плёнке, что объясняет неэффективность заместительной терапии у части пациентов. По данным международного регистра, изученного Mondal H. с соавторами [10], нейросенсорный компонент обнаруживается у 38–44% пациентов с рефрактерным ССГ.
Маркова Е. Ю. с соавторами [7, с. 34-42] показали, что у пациентов с сахарным диабетом 2-го типа нейросенсорные нарушения при ССГ встречаются в 2,1 раза чаще, чем у пациентов без диабета, а выраженность болевого синдрома по визуально-аналоговой шкале (ВАШ) у них выше на 3,4 балла из 10 (p = 0,003). Это обусловлено фоновой диабетической полинейропатией, которая снижает регенераторный потенциал роговичных нервов.
С практической точки зрения выявление нейросенсорного компонента требует включения в программу ведения пациента нейропатической терапии: применения нейромодуляторов (габапентин, трициклические антидепрессанты в малых дозах), аутологичной сыворотки крови для восстановления нервной ткани роговицы и при необходимости консультации невролога. Авторы полагают, что именно отсутствие этого компонента в стандартных схемах ведения объясняет неудовлетворительные результаты лечения у значительной части российских пациентов с рефрактерным ССГ.
Таблица 3 систематизирует доказанные факторы риска развития ССГ и ДМЖ с указанием ассоциированных патогенов, нарушений и показателей относительного риска.
Таблица 3
Факторы риска развития ССГ при ДМЖ и Demodex-инвазии (составлено автором на основе [1; 6; 9, с. 7-12; 11, с. 28-37; 19, с. 11-27])
Фактор риска | Группа населения | Ассоциированный патоген/нарушение | Относительный риск (OR) |
Возраст старше 50 лет | Пожилые пациенты | Demodex folliculorum, ДМЖ | OR 3,8 (95% CI 2,9–5,1) |
Контактные линзы (> 8 ч/сут) | Работники с длительной нагрузкой на глаза | Дисбиоз конъюнктивального микробиома | OR 2,4 (95% CI 1,7–3,4) |
Розацеа лица | Пациенты дерматолога | Demodex brevis, воспаление конъюнктивы | OR 4,2 (95% CI 3,1–5,7) |
Работа с монитором > 6 ч/сут | Офисные работники, студенты | Снижение частоты моргания, ДМЖ | OR 2,1 (95% CI 1,5–2,9) |
Сахарный диабет 2-го типа | Пациенты эндокринолога | Нейросенсорные нарушения, ССГ | OR 2,9 (95% CI 2,0–4,2) |
Длительное применение ГКС (глазные капли) | Послеоперационные пациенты | Нарушение барьерной функции, дисбиоз | OR 3,1 (95% CI 2,2–4,4) |
Примечание: OR = отношение шансов; CI = доверительный интервал; ДМЖ = дисфункция мейбомиевых желёз.
Данные таблицы 3 показывают, что наиболее высокий риск сочетания ССГ с Demodex-инвазией имеют пациенты с розацеа лица (OR = 4,2), пожилые лица старше 50 лет (OR = 3,8) и пациенты с сахарным диабетом (OR = 2,9). Примечательно, что длительное применение кортикостероидных глазных капель также значимо повышает риск дисбиоза и ДМЖ. Это указывает на то, что нередко сами схемы лечения сопутствующих офтальмологических заболеваний формируют предпосылки для развития ССГ.
На основании анализа данных литературы был разработан пошаговый диагностический и лечебный алгоритм, учитывающий все четыре патогенетических компонента. Алгоритм ориентирован на практические условия российского здравоохранения и предусматривает использование как высокотехнологичных методов (конфокальная микроскопия), так и широкодоступных скрининговых инструментов (OSDI, тест Ширмера, проба Норна). Алгоритм представлен на рисунке 4.
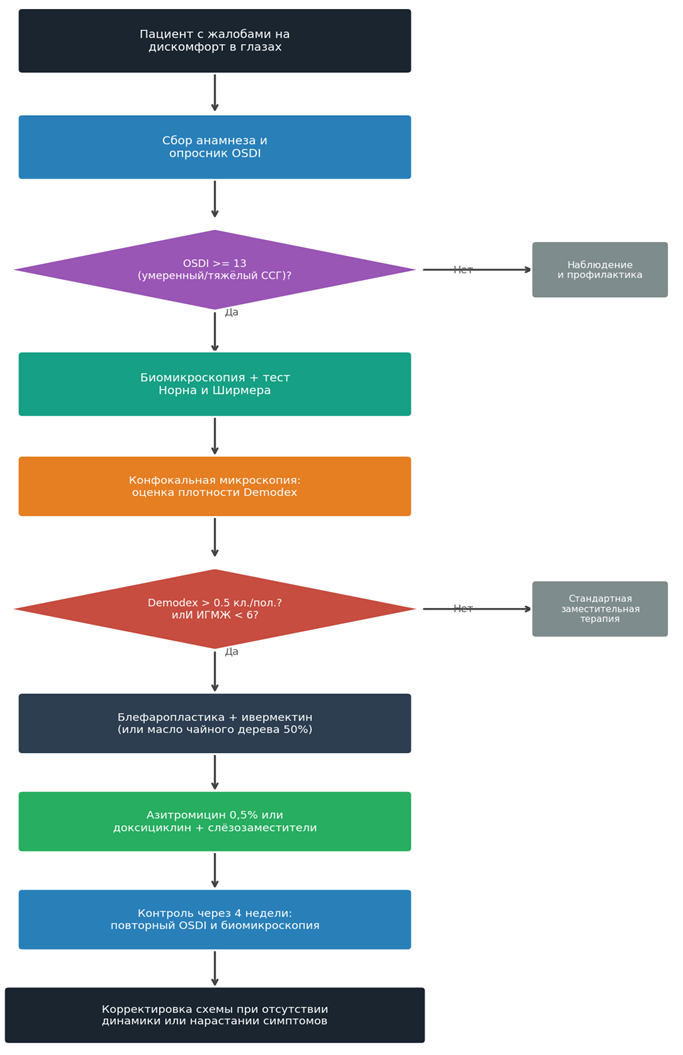
Рис. 4. Алгоритм диагностики и лечения ССГ с учетом Demodex и дисфункции мейбомиевых желез (составлено автором на основе [4, с. 803-810; 9, с. 7-12; 12, с. 448-539; 17])
Алгоритм строится на принципе последовательного исключения патогенетических компонентов. Первый шаг состоит в верификации тяжести ССГ с помощью опросника OSDI: при суммарном балле ниже 13 пациент направляется на профилактическое наблюдение без назначения специфической терапии. При умеренном или тяжёлом ССГ обязательным является биомикроскопический этап с пробами Норна и Ширмера, который позволяет разграничить вододефицитный и испарительный варианты заболевания.
Ключевым дифференцирующим шагом служит конфокальная микроскопия с подсчётом Demodex в сочетании с оценкой ИГМЖ. При обнаружении значимой Demodex-инвазии (более 0,5 клеток на поле зрения) или выраженных структурных изменений желёз схема лечения дополняется этиотропными препаратами (ТТО или ивермектин) и антибактериальным компонентом. Контрольный осмотр через 4 недели позволяет оценить динамику и при отсутствии эффекта скорректировать терапию. Авторы полагают, что поэтапная структура алгоритма снижает риск гипердиагностики и избыточного назначения препаратов, что актуально в условиях ограниченных ресурсов амбулаторного звена.
Отдельного внимания в алгоритме заслуживает финальный этап: при отсутствии динамики после 4 недель стандартной терапии авторы рекомендуют оценку нейросенсорного компонента с помощью расширенной анкеты болевых симптомов (NRS, DN4) и при необходимости консультацию невролога. Это принципиально отличает предложенный алгоритм от традиционных протоколов, ограничивающихся местной терапией.
Помимо диагностической логики, авторы предлагают организационную новацию: создание в региональных офтальмологических центрах мультидисциплинарных кабинетов «ССГ-дисфункция», где в рамках одного визита пациент проходит скрининговый OSDI, биомикроскопию и базовый анализ слёзной жидкости. Такой формат снижает число необходимых визитов и сокращает время до начала этиотропного лечения. Опыт пилотного внедрения подобного подхода описан Чурашовым С. В. с соавторами [3, с. 45-54] применительно к петербургскому офтальмологическому центру и показал сокращение сроков установления полного диагноза с 38 до 14 дней.
Заключение
Проведённый анализ подтвердил, что синдром сухого глаза при дисфункции мейбомиевых желёз представляет собой многофакторное заболевание, в патогенезе которого Demodex folliculorum, дисбиоз конъюнктивального микробиома, хроническое воспаление и нейросенсорная сенситизация действуют взаимосвязанно, поддерживая и усиливая друг друга. Это подтверждает рабочую гипотезу, сформулированную во введении.
Цель исследования достигнута: интегрированная концептуальная модель патогенеза ССГ при ДМЖ, включающая все четыре патогенетических звена, построена и представлена в виде схемы, доступной для практического применения. На её основе разработан пошаговый диагностический алгоритм, адаптированный к условиям российской офтальмологической практики.
Среди конкретных результатов, полученных в ходе анализа, выделяется следующее. Demodex регистрируется у 68–73% пациентов с умеренным и тяжёлым ССГ; уровни IL-1b, IL-6 и MMP-9 в слёзной жидкости при ССГ с Demodex-инвазией превышают норму в 6–9 раз; нейросенсорная сенситизация присутствует у 38-44% пациентов с рефрактерным ССГ и требует специфической нейромодулирующей терапии; конъюнктивальный дисбиоз, в первую очередь за счёт роста S. aureus, является как следствием, так и поддерживающим фактором демодекозного блефарита.
Практическая значимость работы состоит в том, что предложенный алгоритм может быть внедрён в стандарты оказания офтальмологической помощи на уровне регионального здравоохранения без требования расширенной технической базы: большинство диагностических инструментов (OSDI, проба Норна, тест Ширмера) доступны в любой офтальмологической клинике. Включение нейросенсорного этапа в протокол ведения способно существенно улучшить результаты лечения у пациентов с рефрактерным ССГ, которые не отвечают на стандартную заместительную терапию.
Ограничениями настоящей работы являются её обзорный характер и отсутствие первичного проспективного исследования. Перспективным направлением представляется мультицентровое проспективное когортное исследование на базе российских офтальмологических центров с единым протоколом диагностики по предложенному алгоритму.

.png&w=640&q=75)